مقدمه
درد حین یا چند روز قبل از قاعدگی یا دیسمنوره از شایعترین اختلالات قاعدگی است. دیسمنوره به دو دسته تقسیم می شود: دیسمنوره ثانویه که به دلیل علتهای زمینهای مثل آدنومیوز، اندومتریوز، بیماری التهابی لگن و یا لیومیومهای رحمی بروز میکند و دیسمنوره اولیه که شایعتر است و بدون هیچ علت ارگانیک در زمان قاعدگی و بیشتر در دختران جوان دیده میشود [1]. این مشکل علاوه بر کاهش کیفیت زندگی، باعث اختلال در فعالیتهای اجتماعی و شغلی زنان نیز میشود، به گونهای که برآورد شده در ایالات متحده آمریکا این عارضه باعث 600 میلیون ساعت ترک کار و 2 میلیارد دلار هزینه سالانه میگردد؛ فارغ از اینکه زنانی که ترک کار ندارند نیز دچار کاهش بازدهی و کیفیت کار میشوند [2].
شیوع دیسمنوره در مطالعات مختلف، از 16 درصد تا 91 درصد گزارش شده است [3]. شیوع این مسئله در ایران نیز حدود 71 درصد بیان شده است [4]. یکی از اتفاقاتی که در افراد مبتلا به دیسمنوره مشاهده شده است، ترشح بیش از حد یا غیرمتعادل پروستانوئیدها از اندومتر رحم بهویژه اندومتر ترشحی در طول دوره قاعدگی است. این اتفاق زمینهساز افزایش انقباضات بدون ریتم رحمی، افزایش تون پایه رحم و درنهایت کاهش خونرسانی بافت رحم و افزایش حساسیت اعصاب محیطی میشود. البته کاهش پروژسترون در فاز تأخیری لوتئال و تحریک آنزیمهای تولیدکننده آراشیدونیک اسید و فعالسازی مسیر سیکلواکسیژناز در این اتفاقات بسیار دخیل هستند، به گونهای که داروهای ضدالتهاب غیراستروئیدی مهمترین دسته دارویی مورد استفاده در درمان دیسمنوره هستند، چراکه مهارکننده سیکلواکسیژناز هستند [1].
خط اول درمان دیسمنوره داروهای ضدالتهابی غیراستروئیدی هستند و انتخاب از بین داروهای مختلف این دسته دارویی به تحمل و پاسخ بیمار بستگی دارد. به جز داروهای ضدالتهابی غیراستروئیدی درمانهای خوراکی و غیرخوراکی دیگری نیز برای دیسمنوره اولیه پیشنهاد شده است که هنوز شواهد کافی برای تأیید اثربخشی آنها وجود ندارد [5].
مطالعه مروری کاکران نشان داده که تاکنون درمانهای خوراکی متعدد گیاهی و غیرگیاهی برای تسکین دیسمنوره مورد مطالعه قرار گرفتهاند. از ترکیبات غیرگیاهی میتوان به روغن ماهی، ملاتونین، ویتامین B1، ویتامین E و زنیک سولفات اشاره کرد و از درمانهای گیاهی به بابونه، دارچین، گل سرخ، شوید، رازیانه، شنبلیله، زنجبیل، سنبلالطیب، آویشن و ریواس. البته این مطالعه مروری روشمند ذکر میکند که هنوز شواهد کافی برای ترجیح این درمانها نسبت به داروهای ضدالتهابی غیراستروئیدی وجود ندارد [6].
درمانهای غیرخوراکی مختلفی نیز برای دیسمنوره اولیه پیشنهاد شدهاند که شواهد برای اثبات تأثیر آنها نیز کافی نیست مثل حرارت موضعی، طب سوزنی، یوگا، ماساژ و ورزش [11-7].
گیاهان دارویی متعددی در سراسر دنیا برای درمان اختلالات قاعدگی و تسکین دیسمنوره استفاده میشوند، مثلاً تایند وان اندل و همکاران در یک مطالعه مروری بیان کردند که فقط در آمریکای لاتین، کارائیب، جنوب صحرای آفریقا، جنوب و جنوب شرقی آسیا بیش از 2000 گیاه برای درمان اختلالات قاعدگی استفاده میشوند که بیشتر آنها برای درمان دیسمنوره، آمنوره، قاعدگی نامنظم و یا القای سقط هستند. آنها آثار فارماکولوژیک تعدادی از داروهای پرتکرار را بررسی کرده و متوجه شدند که حدود 50 درصد از آنها ضداسپاسم و در کمال تعجب حدود 30 درصد از آنها اسپاسم ایجاد میکنند. نکته حائز اهمیت دیگری که این مطالعه بیان شده بود، سمیت درخور توجه تعداد قابل توجهی از این داروها بود که اهمیت بررسی دقیق و علمی آنها را روشن میسازد [12].
در ایران داروهای متعددی برای دیسمنوره استفاده میشود، مثلا شجاع و همکاران در تحقیقی از تعدادی از دانشجویان دختر ساکن خوابگاه علومپزشکی دانشگاه گلستان و نیز تعدادی از عطاران گلستانی، از طریق پرسشنامه، متوجه شدند که در مجموع 29 ترکیب گیاهی و غذایی برای این منظور مورد استفاده افراد مبتلاست که بیشترین استفاده مربوط به عرق نعناع، زیره، چای نبات داغ، گل گاو زبان، آویشن، شیرین بیان، رازیانه، بابونه، بومادران، عناب، گل ختمی، گندنای کوهی، زنجبیل، عرق شاتره، بابونه، برگ پونه، تخم شنبیله، تخم شوید، تخم جعفری، تخم رازیانه، گل کلپوره، سیاهدانه، گز علفی و عرق چهلگیاه است [13].
یکی از گیاهان دارویی که در منابع طب سنتی، تسکیندهنده درد شناخته میشود گیاه بابونه است [14]. بابونه با نام علمی Matricaria Chamomilla از شناختهشدهترین گیاهان دارویی در سراسر جهان است. عصاره آبی و اتانولی گلهای این گیاه اثر ضدالتهاب، ضداسپاسم، آرامبخشی و کاهنده بیقراری دارد [15]. مطالعات نشان داده که استفاده از بابونه میتواند به کاهش درد شکم و لگن در هنگام قاعدگی و همچنین کاهش علائمی مثل خستگی، بیحالی و افسردگی کمک کند [16 ،15 ،1]. در مطالعهای در آمریکا حدود 50 درصد از زنان به طور تجربی از چای بابونه جهت تسکین دسیمنوره استفاده کرده بودند. عوارض جانبی بابونه نادر است و گاه واکنشهای آلرژیک ایجاد میکند که اکثراً محدود است [15]. در مطالعات مصرف بابونه به صورت چای تا 20 گرم در روز گزارش شده است [۱۸ ،۱۷].
یکی دیگر از گیاهان دارویی که اثرات تسکیندهنده درد آن شناخته شده، گیاه زنجبیل است [19]. ریشه گیاه زنجبیل، یک ادویه غذایی پرکاربرد است که سازمان غذا و داروی آمریکا (FDA) آن را به عنوان مکمل غذایی و نیز یکی از داروهای بسیار کمعارضه در نظر گرفته است [20]. جینجرول یکی از مواد تشکیلدهنده زنجبیل است که خاصیت ضددرد، آرامبخش، ضدتب و ضدباکتری درحیوانات دارد. اثر ضدالتهاب زنجبیل ناشی از مهار سیکلواکسیژناز و لیپواکسیژناز و به دنبال آن کاهش لکوترین و پروستاگلاندین است [21]. درباره اثرات زنجبیل بر دیسمنوره نیز مطالعات متعددی صورت گرفته است و اثربخشی آن را در دیسمنوره مشابه داروهای ضدالتهابی غیراستروئیدی دانستهاند. در این مطالعات زنجبیل با دوز250 میلیگرم تا 2 گرم در روز استفاده شده است [۲۵-۲۱].
عسل از مهمترین مواد قندی طبیعی است که تاکنون 15 نوع قند در آن کشف شده و لذا سرشار از انرژی و حرارت است [26]. به عسل از دیرباز نهتنها به عنوان ماده غذایی ارزشمند، بلکه به منزله دارو توجه شده است. در طب جدید نیز اثرات درمانی عسل موجب شده که عسل در بسیاری از کشورها به عنوان غذادارو به رسمیت شناخته شود [27]. از عسل در درمان دیسمنوره اولیه نیز استفاده میشود. عسل به واسطه وجود آنزیمها و املاح معدنی در کاهش درد و گشادی رگها مؤثر است. عسل خالص غلظت پروستاگلاندین E2 و پروستاگلاندین آلفا-2 و ترومبوکسان B2 را در خون کاهش میدهد و در نتیجه در کاهش دردهای قاعدگی مؤثر است [28].
با توجه به شیوع بالای دیسمنوره و علائم همراه با آن در ایران، اهمیت تسکین درد دیسمنوره با ترکیبات کمعارضه، وفور و تنوع گیاهان دارویی در کشور، گرایش عمومی به استفاده از داروهای گیاهی، عوارض جانبی داروهای موجود و لزوم تکرار دورههای مصرف، هزینه گزاف تهیه مواد اولیه داروهای شیمیایی از کشورهای خارجی، منع مصرف داروهای موجود در برخی از افراد، انجام مطالعات کنترلشده در زمینه تأثیر بابونه و زنجبیل بر دیسمنوره را پراهمیت کرده است. همچنین نبود مطالعه مقایسهای در زمینه اثرات ترکیب زنجبیل و بابونه با عسل بر دیسمنوره و علائم همراه آن باعث شده که در مطالعه حاضر با هدف تحکیم نتایج قبلی و یا یافتن نتایج جدید، به بررسی تأثیر ترکیب بابونه و زنجبیل (به صورت جوشانده) با عسل بر شدت درد دیسمنوره اولیه و علائم همراه آن، در مقایسه با بابونه (به صورت جوشانده) به همراه عسل، زنجبیل (به صورت جوشانده) به همراه عسل و کپسول مفنامیک اسید در دانشجویان دختر دانشگاههای شهر اراک بپردازیم.
مواد و روشها
این مطالعه، کارآزمایی بالینی کنترلشده تصادفی مبتنی بر رضایت آگاهانه است که روی 400 نفر از دختران دانشجوی دانشگاههای شهر اراک، شامل دانشگاه علومپزشکی اراک، دانشگاه آزاد، دانشگاه فرهنگیان و دانشگاه عالی علوم، در سال تحصیلی 1396-1395 انجام گرفت. روش انتخاب نمونهها به روش آسان از جامعه مدنظر بود.
حجم نمونه با استفاده از فرمول مقایسه میانگینها و با درنظرگرفتن سطح اطمینان 95 درصد و توان 80 درصد و اندازه اثر 70 درصد محاسبه شد که برای هر گروه 70 نفر در نظر گرفته شد . با ضریب ریزش 40 درصد، این عدد به 100 افزایش داده شد. در ابتدا از کل دانشجویان دختر (1278 نفر) که به هنگام قاعدگی درد داشتند، 513 نفر از کسانی که معیارهای ورود را داشتند، وارد مطالعه شدند. از بین آنها 400 نفر که تمایل به شرکت در طرح داشتند، انتخاب شدند. دانشجویان شرکتکننده (400 نفر) با استفاده از بلوکهای تصادفی در چهار گروه تقسیم شدند، به طوری که در هر گروه 100 دانشجو به طور تخصیص تصادفی قرار داده شدند (تصویر شماره 1).
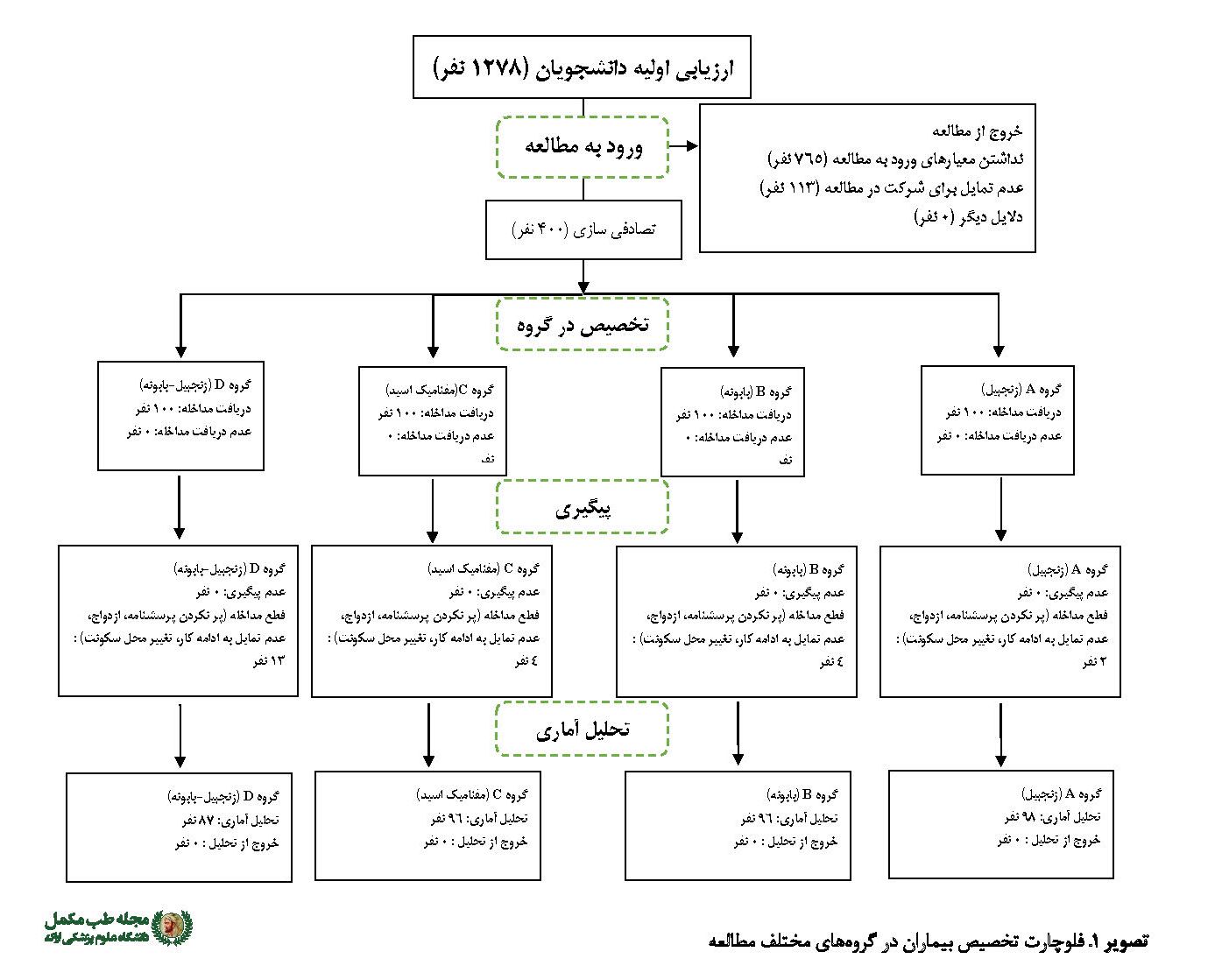
معیارهای ورود به مطالعه عبارت بودند از: سن 18 تا30 سال، مجردبودن، شروع درد قاعدگی قبل از 20سالگی (دیسمنوره اولیه معمولاً دختران زیر 20 سال را درگیر میکند)، تجربه درد و علائم دیسمنوره متوسط و شدید از چند ساعت قبل از خـــــونریزی تا حداکثر روز پنجم، خـــــونریزی ماهیانه و منظم بودن آن با فواصل 21 تا 35 روز، خـــــونریزی کم و متوسط در دوران قاعدگی (نبود دفع لخته)، مبتلانبودن به بیماریهای مزمن (دیابت، پرکاری وکمکاری تیروئید، بیماری مزمن کبدی یا کلیوی و افسردگی تشخیصدادهشده)، نداشتن سابقه زخم معده یا دوازدهه، نداشتن سابقه مثبت بیماریهای التهابی لگن، میوم و تومورهای لگنی، نداشتن سابقه جراحیهای زنان یا جراحی شکمی (شامل هر نوع جراحی باز یا لاپاراتومی و لاپاراسکوپی در ناحیه لگن مانند کیست، توده، چسبندگی)، استفادهنکردن از داروهای ضدبارداری خوراکی، داروهای خانواده بنزودیازپینها، باربیتوراتها، نارکوتیکها، برخی از ضدافسردگیها مثل فلوکستین و داروهای ضدانعقاد و الکل، نداشتن علائمی مثل سوزش، خارش و ترشح غیرطبیعی در ناحیه تناسلی، نداشتن سابقه آلرژی به گیاهان دارویی، نداشتن تجربه عوامل استرسزای بزرگ مثل جدایی والدین یا فوت بستگان درجه یک در دو ماه اخیر، نداشتن اجبار به مصرف دارو یا رژیم غذایی خاص، نکشیدن سیگار، نداشتن برنامه برای انتقال، جابهجایی، میهمانی در دانشگاه دیگر یا فارغالتحصیلی طی شش ماه بعد از شروع مطالعه و نداشتن تجربه درد در تمام سیکل یا تمام مدت خـــــونریزی.
در طول مطالعه بیماران از طریق گروهی در یکی از پیامرسانهای اجتماعی با محققان در تماس بودند و از این طریق سؤالات خود را میپرسیدند و پیگیریهای لازم از طریق تلفن و پیامرسان اجتماعی انجام میشد. معیارهای خروج از مطالعه نیز عبارت بودند از: تمایل شخصی برای خروج از مطالعه، مصرف نامنظم داروها بر اساس خوداظهاری، بروز استرس زیاد در طول مطالعه (مثل فوت اعضای درجه اول خانواده یا جدایی والدین)، ایجاد نیاز به مصرف طولانی یا مداوم دارو و مکملهای غذایی و ویتامینها در طول مطالعه بر اساس تشخیص پزشک، انجام هر نوع جراحی در طول مطالعه، ازدواج در طول دوره مطالعه یا تغییر محل سکونت، امتناع از پرکردن پرسشنامه، تمایل به قطع مصرف دارو به هر دلیل (نظیر بروز عوارض شدید و یا رضایتنداشتن)، مصرفنکردن دارو طبق دستورالعمل و پرنکردن چارتها طبق دستورالعمل چاپی دادهشده به بیماران.
پس از اخذ مجوز کمیته اخلاق دانشگاه و دریافت معرفینامه از دانشکده پرستاری و مامایی اراک و ارائه آن به مسئولان مربوط در دانشگاهها، همکار نمونهگیر طرح، بهنوبت برای نمونهگیری به دانشگاههای اشارهشده مراجعه کرد و بعد از توضیح هدف پژوهش و نحوه اجرا، اثرات داروهای مصرفی و نحوه پرکردن پرسشنامه و استفاده از خطکش درد برای دانشجویان، از آنهایی که به هنگام قاعدگی درد داشتند، برای پیوستن به طرح دعوت کرد. در صورت رضایت جهت شرکت در مطالعه، مشخصات جمعیتشناختی، شدت دیسمنوره و سایر اطلاعات ضروری از طریق پرسشنامه شماره یک و خطکش درد بررسی شدند و درد قاعدگی آنها در یک سیکل قاعدگی سنجیده شد و از نمونهها خواسته شد عدد دردی را که احساس میکنند، روی خطکش درد علامت بزنند. نمونههایی که میانگین درد قاعدگی 4 یا بیشتر از 4 داشتند (دیسمنوره متوسط و شدید) و بقیه معیارهای ورود به مطالعه را داشتند، به اندازه حجم نمونه مدنظر، برای همکاری دعوت شدند.
در این پژوهش اطلاعات به وسیله یک پرسشنامه اولیه، مقیاس آنالوگ بصری، چارت هیگام و مقیاس کلامی آندرش ـ میلسوم گردآوری شد. پرسشنامه اول مشتمل بر اطلاعات جمعیتشناختی، تاریخچه قاعدگی، ورزش منظم، سابقه بیماریهای مزمن، سابقه مصرف داروی خاص، سیگار، الکل سابقه جراحی زنان، ترشح واژینال غیرطبیعی و سابقه آلرژی به گیاهان دارویی بود.
شدت درد دیسمنوره با مقیاس آنالوگ بصری (واس) اندازهگیری شد. مقیاس سنجش شدت درد مدرج (خطکش درد) خط افقی10 سانتیمتری است که در انتهای چپ آن واژه «بدون درد» و در انتهای راست آن واژه «بیشترین درد قابل تصور» درج شده است و دانشجو روی این خطکش میزان درد را مشخص کرد. شدت درد بدین صورت طبقهبندی و ارزیابی شد: الف. درد شدید (امتیازدرد 10-8 و نیاز به محدودیت فعالیت، استراحت و مصرف مسکن)، ب. درد متوسط (امتیاز درد 7-4 و نیاز به مصرف مسکن)، ج. درد خفیف (امتیاز درد 3-0 و نبود نیاز به مسکن و استراحت) [29].
علائم همراه با دیسمنوره بر اساس مقیاس کلامی آندرش ـ میلسوم سنجیده شد. در این مقیاس، 4 درجه برای شدت علائم همراه دیسمنوره ذکر شده است: 0: علائم وجود ندارد. 1: علائم خفیف است و با کارهای روزمره تداخلی ندارد. 2: علائم متوسط وجود دارد که با کارهای روزمره تداخل دارد ولی ناتوانکننده نیست. 3: علائم شدید و کاملاً ناتوانکننده است [30].
جهـــــت تعیـــــین مقـــــدار خـــــونریزی از چارت هیگام اسـتفاده شـد که چـارت تصویری برای ارزیابی میزان خون ازدسـترفتـه قاعـدگی است. در این چارت به نوار بهداشتی با آغشتگی به لکههای خونی کوچک، امتیاز 1، آغشتگی نیمی از نوار، امتیاز 5 و آغشتگی کامل به خون، امتیاز 20 تعلق میگیرد. همچنین به لختهها بر اساس اندازهشان امتیـازی بین 1 تا 5 داده میشـود. بدین صورت که در این چارت تصویری که یک جدول دوبعدی است، در ردیف افقی تعداد روزهای قاعدگی و در ردیف عمودی دیاگرام پدهای آغشته به خون را بعد از هر بار تعویض پد، بر حسب میزان آغشتگی پدها به خون در درون چارت، در خانه مربوط به همان روز از قاعدگی در سه درجه خفیف، متوسط و شدید علامت خواهند زد.
در پایان قاعدگی هر علامت را در امتیاز مربوط ضرب میکنند و اعداد بهدستآمده را با هم جمع کرده و امتیاز کلی محاسبه میشود. امتیـاز زیـر 50 نشاندهنده خـــــونریزی خفیف، امتیاز 100-51 نشانگر خـــــونریزی متوسط و امتیاز 100 به بالا نمایانگر خـــــونریزی شـدید هنگـام قاعدگی است. طول مدت خـــــونریزی نیز در این چارت ثبت شد [31].
پرسشنامه اول و سایر چارتها و پرسشنامهها قبل از شروع مداخله، یک و دو ماه پس از مداخله توسط واحدهای پژوهش تکمیل شد. داوطلبانهبودن شرکت در پژوهش و محرمانهبودن اطلاعات اخذشده، تأکید بر مختاربودن نمونهها برای انصراف از مطالعه در هر مرحله از تحقیق، به واحدهای پژوهش یادآوری شدو پس از تکمیل رضایتنامه، به اسامی دانشجویان شماره داده شد و پرسشنامههای دوم و سوم با ذکر شمارهها نامگذاری شد. در مرحله بعد با توجه به دادههای نمونهها و راهنمایی مشاور آمار مشابهسازی انجام شد و دانشجویان با استفاده از بلوکهای تصادفی در چهار گروه تقسیم شدند، به طوری که در هر گروه 100 دانشجو به طور تصادفی قرار گرفتند.
برای افراد تحت مطالعه، پدهای بهداشتی بالدار متوسط بدون ماده جاذب با برند یکسان (مای لیدی) جهت استفاده حین قاعدگی تهیه شد تا افراد در همه گروهها شرایط یکسان و قابل سنجشی به منظور تخمین میزان خـــــونریزی قاعدگی داشته باشند. پدهای بهداشتی برای مدت سه سیکل (یک ماه قبل از شروع مداخله و دو ماه بعد از شروع مداخله) و تمامی چارتهای لازم در طول مطالعه به صورت چاپشده در اختیار شرکتکنندگان قرار گرفت.
گیاهان دارویی پس از تهیه از بازار تهران، توسط داروساز سنتی شناسایی و تأیید شدند. استانداردسازی تمام داروها، آزمایشهای کنترل میکروبی و آزمایش پایداری مواد مؤثره دارو توسط داروساز سنتی در آزمایشگاه فارماسوتیک دانشگاه علوم پزشکی تهران تأیید شد و استانداردسازی بر اساس اسانس صورت گرفت. ترکیبات اسانس توسط داروساز سنتی توسط دستگاه GC-MS شناسایی شد. نتایج GC/MS برای بابونه نشان داد که آلفاـ بیزابولول اکسید مهمترین جزء فرآورده است (34 درصد) و سپس کامازولن (12 درصد)، 1و 8 ـ سینئول (8 درصد) و لیمونن (5 درصد) بیشترین اجزا بودند. نتایج آنالیز زنجبیل نشان داد بیشترین جزء آن آلفاـ زینجیبرین (22 درصد) است و سپس بتاـ سزکوئی فلاندرن (9 درصد)، 1و8 ـ سینئول (8 درصد) و آلفاـ فرانسن (7 درصد) هستند.
پس از توزین، داروهای هر گروه در پلاستیکهای زیپکیپ ریخته شد. هر زیپکیپ به ترتیب حاوی موارد زیر بود: افراد گروه A، 1000 میلیگرم پودر ریشه زنجبیل همراه با 50 گرم عسل، افراد گروه B، 5000 میلیگرم بابونه همراه با 50 گرم عسل، افراد گروه C، 15 عدد کپسول مفنامیک اسید 250 میلیگرم، افراد گروه D، 1000 میلیگرم پودر ریشه زنجبیل و 5000 میلیگرم بابونه همراه با 50 گرم عسل. به منظور کورسازی، داروها به مقدار نیاز یک سیکل (15 عدد زیپکیپ یا 15 عدد کپسول)، داخل جعبههای مقوایی مشابه در اختیار شرکتکنندگان قرار داده میشد و محققان و شرکتکنندگان از محتویات جعبهها اطلاعی نداشتند. بیمار باید محتویات هر زیپکیپ را با 150 سیسی آب به مدت 3 دقیقه با حرارت ملایم میجوشاند، سپس آن را صاف کرده و با یک قاشق مرباخوری عسل حل کرده و میل مینمود.
برای افراد گروه C کپسولهای مفنامیک اسید با دوز250 میلیگرم از شرکت دارویی رها تهیه و تجویز شد. دستورالعمل تجویز در همه گروهها به طور یکسان به مدت 2 روز قبل از قاعدگی تا 3 روز بعد از شروع قاعدگی و روزانه 3 نوبت بعد از غذا برای دو سیکل متوالی بود. از هر گروه درخواست شد داروها را طبق دستور مصرف کنند و مصرف صحیح و بهموقع داروها به طور مکرر پیگیری شد و از آنها درخواست شد در طی زمان قاعدگی با دقت زیاد چارتهای مدنظر در پرسشنامهها را تکمیل کنند و در صورت وجود هر گونه سؤال یا مشکل با پژوهشگر در ارتباط باشند. شدت درد دیسمنوره با خطکش درد (واس) اندازهگیری شد که بیمار در زمان مصرف اولین دوز دارو ـ 2 ساعت، 4 ساعت، 6 ساعت و 8 ساعت بعد از مصرف اولین دوز دارو ـ شدت درد را در جای تعیینشده در مقیاس دیداری درد علامت میزد.
به علت اینکه داوطلبان از دیسمنوره متوسط تا شدید رنج میبردند، جهت رعایت ملاحظات اخلاقی برای تسکین درد، داوطلبان در صورت نیاز میتوانستند از مسکنهای دیگر در صورت کنترلنشدن درد استفاده نمایند و نوع و تعداد مصرف مسکنها را حتماً به طور دقیق ثبت مینمودند. پس از سیکل اول و دوم از مصرف داروها توسط واحدهای پژوهش، بهترتیب تمامی چارتها تکمیل شده و جمعآوری شد. سپس دادهها با استفاده از نرمافزار آماری SPSS نسخه 19 مطابق با اهداف پژوهش، با استفاده از تستهای آماری کروسکال والیس، کای اسکوئر، فیشر، فریدمن، تحلیل واریانس با اندازهگیری های مکرر در سطح معنیداری 0/05 تجزیه و تحلیل شدند.
یافتهها
در طول مطالعه 23 نفر به دلیل پرنکردن پرسشنامه، ازدواج، تمایلنداشتن به ادامه کار و قطع دارو از مطالعه خارج شدند. در مجموع عوارض گزارششده از داروها عبارت بودند از حساسیت پوستی (17 نفر)، عوارض گوارشی (18 نفر) و گُرگرفتگی (9 نفر) که بیشترین عوارض مربوط به گروه زنجبیل بود. البته عوارض در حدی نبودند که باعث خروج از مطالعه شوند. عارضه گرگرفتگی محدود به گروههای مصرفکننده زنجبیل و ترکیب بابونه و زنجبیل بود و حساسیت پوستی نیز بیشتر از همه در مصرفکنندگان زنحبیل دیده شد.
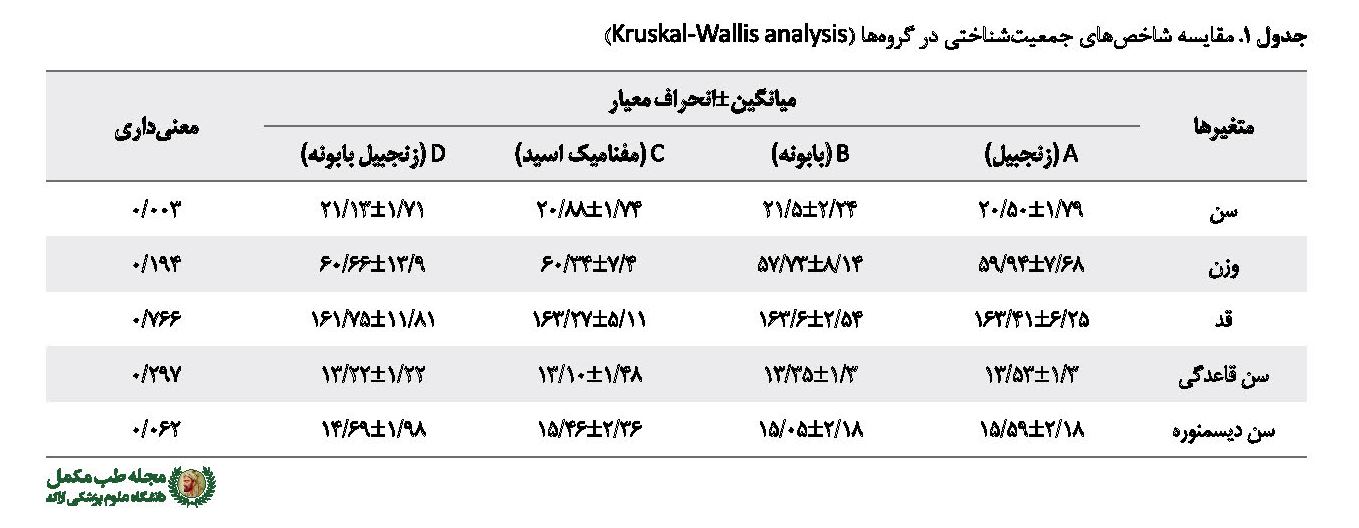
بیشترین عارضه گوارشی نیز در مصرفکنندگان مفنامیک اسید بروز کرده بود. کمترین عوارض مربوط به مفنامیک اسید بود، ولی در مجموع تفاوت آماری معنیداری بین گروهها در ارتباط با عوارض مشاهده نشد. درنهایت دادههای 377 نفر تحلیل شد: 98 نفر در گروه A (زنجبیل)، 96 نفر در گروه B (بابونه)، 96 نفر در گروه C (مفنامیک اسید) و 87 نفر در گروه D (بابونه و زنجبیل). میانگین سنی نمونهها 1/91±21/002 سال و در رده سنی 18-30 سال قرار داشتند. میانگین سن قاعدگی 1/31±13/31 سال و در رده 18-9 سال بود.
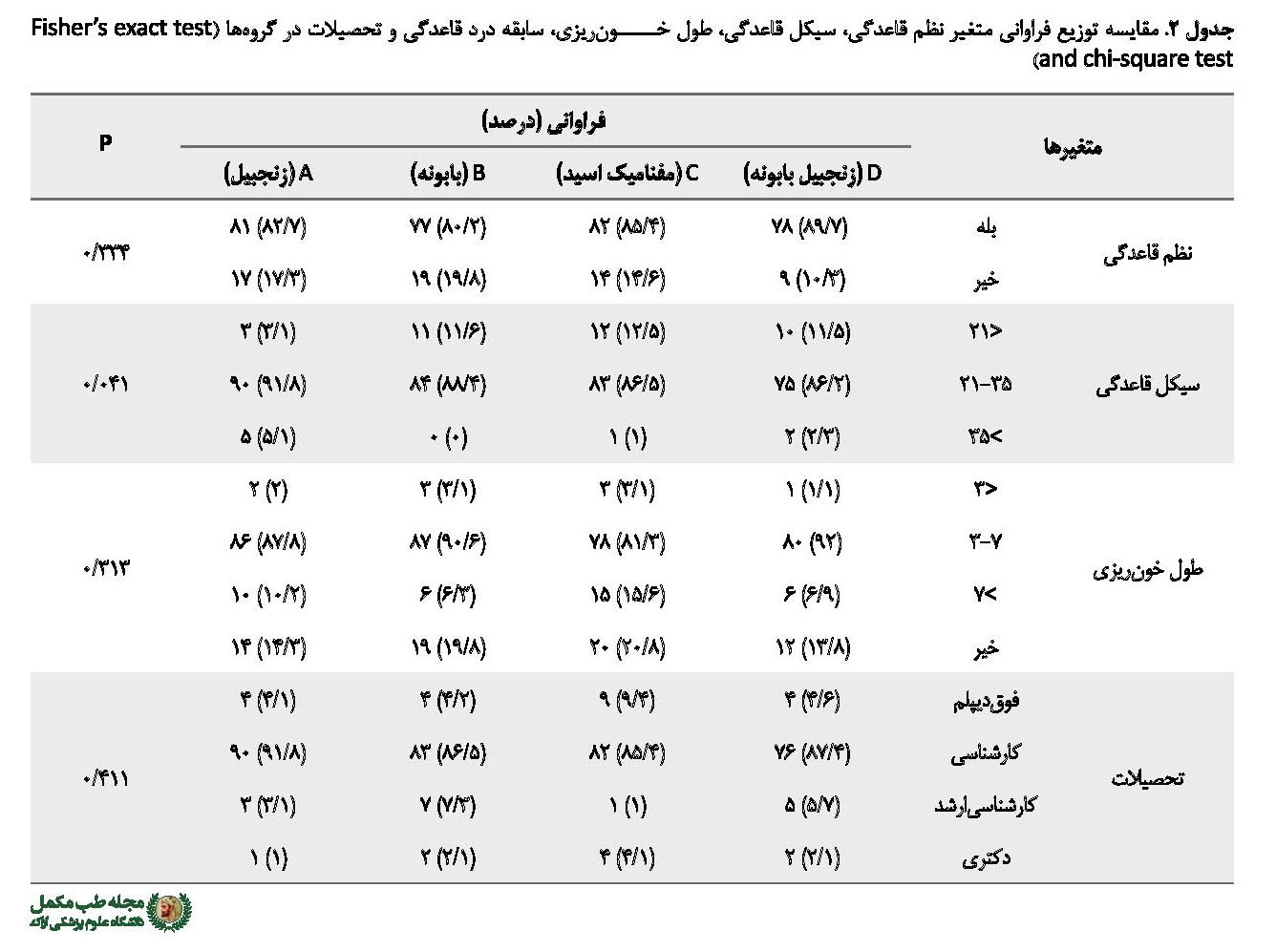
همچنین میانگین سن دیسمنوره 2/21±15/21 سال و در رده سنی 25-10 سال بود. نتایج آنالیز کروسکال والیس نشان داد بجز میانگین سن، میانگین سایر متغیرها مثل وزن، قد، سن قاعدگی و سن دیسمنوره در گروهها با یکدیگر اختلاف معنادار آماری ندارد (جدول شماره 1). نتایج آزمون دقیق فیشر و آزمون کای اسکوئر نیز نشان داد که به جز سیکل قاعدگی، توزیع فراوانی نظم قاعدگی، طول مدت خـــــونریزی، سابقه درد قاعدگی و تحصیلات بین 4 گروه با یکدیگر اختلاف معنادار آماری ندارد (جدول شماره 2).
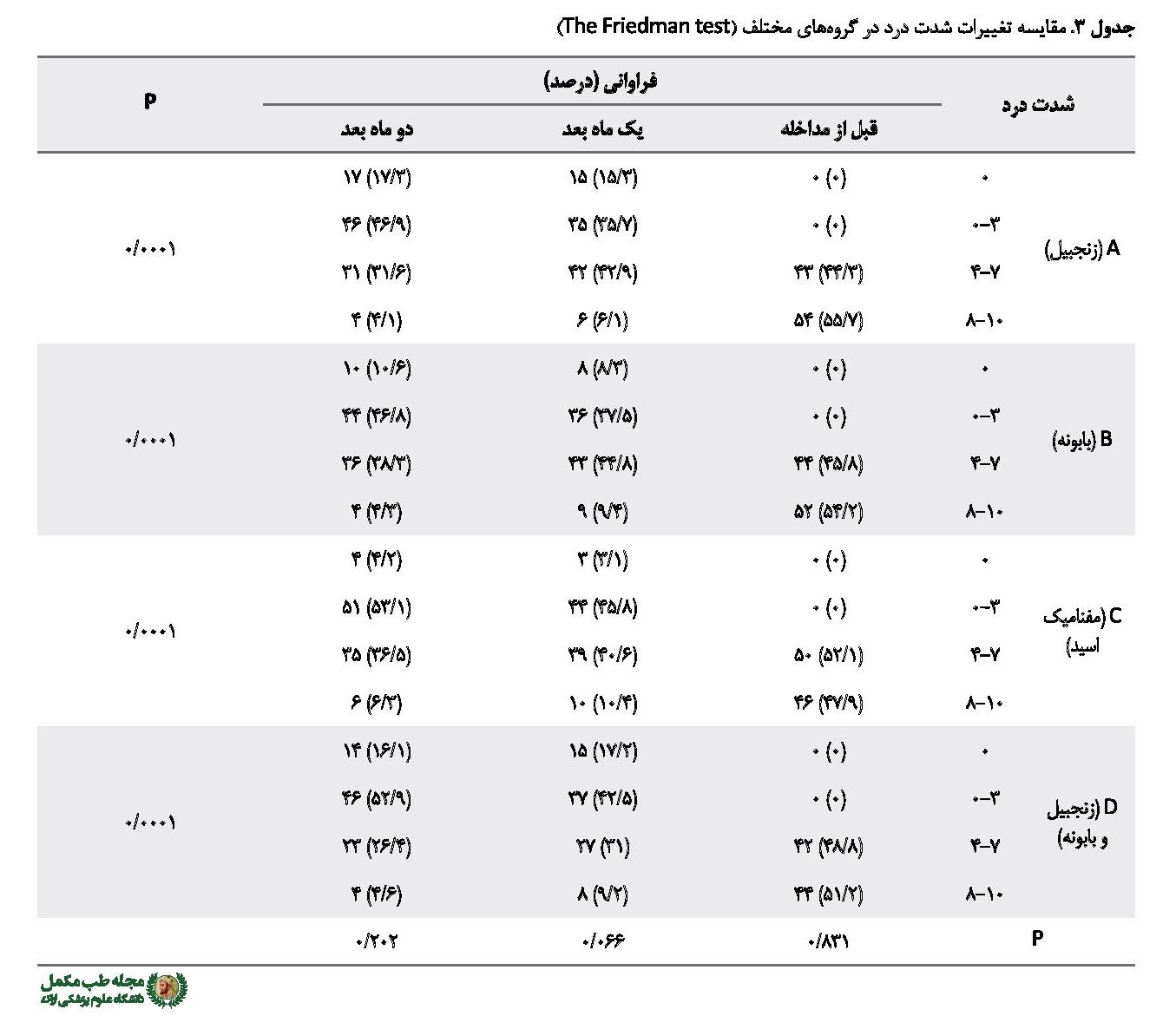
نتایج آزمون دقیق فیشر نشان داد توزیع فراوانی درد به ساعت، در گروهها با یکدیگر اختلاف معنادار آماری ندارد، روند تغییرات در هر 4 گروه بهسمت کاهش مدت زمان درد بود، ولی آزمون فریدمن نشان داد این تغییرات بین 4 گروه تفاوت معناداری ندارد و هر 4 مداخله اثر مشابه داشتند. نتایج آزمون فریدمن نشان داد تغییرات میانگین تعداد روزهای درد در گروهها معنادار وکاهشی بوده، اما نتایج بین گروهی نشان داد میانگین درد در بین گروهها تنها یک ماه بعد با یکدیگر اختلاف معنادار آماری داشته که بیشترین اثر مربوط به زنجبیل بود (0/031=P). تغییرات شدت درد و توزیع فراوانی مصرف مسکن در زمانهای مختلف داخل گروهها معنادار بود و روند کاهشی داشت، اما بین گروهها اختلاف معنادار آماری وجود نداشت و هیچ کدام از مداخلات نسبت به دیگری برتری نداشتند (جدول شماره ۳). آزمون کای اسکوئر نشان داد توزیع فراوانی لکه بینی، توزیع فراوانی دفع لخته، توزیع فراوانی خون جریاندار داخل گروهی و بین گروهی، قبل و بعد از مداخله اختلاف معنادار آماری نداشته است.
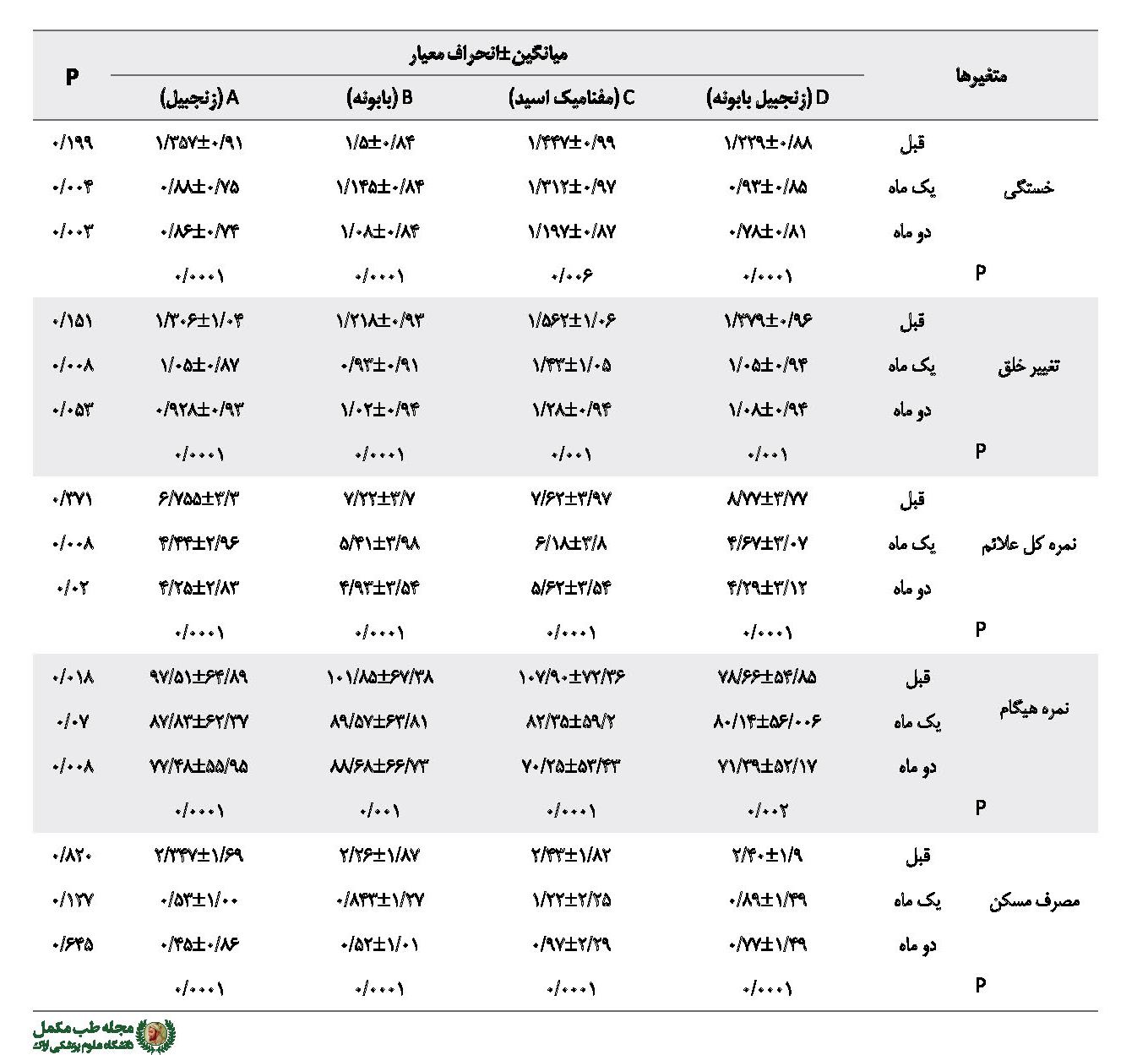
نتایج آزمون آنالیز واریانس نشان داد که میانگین نمره علائم همراه دیسمنوره قبل از مطالعه، بجز اسهال و سردرد، در بقیه موارد تفاوت آماری معناداری نداشت. نمره کل علائم همراه قبل از مطالعه بین 4 گروه تفاوت معناداری نداشت، ولی تغییرات آن در طول مطالعه کاهشی بود و بین 4 گروه تفاوت معناداری وجود داشت (0/02=P) که بیشترین تغییرات مربوط به گروه زنجبیل و بابونه بود و کمترین تغییرات مربوط به گروه مفنامیک اسید. در مورد تکتک علائم نیز روند کاهش در اکثر موارد دیده شد؛ گرچه این تفاوت بین گروهها معنادار نبود، مگر در چند مورد. کاهش سرگیجه، تغییر خلق و لتارژی (بیحالی) یک ماه بعد از مداخله بین گروهها تفاوت معنادار داشت.
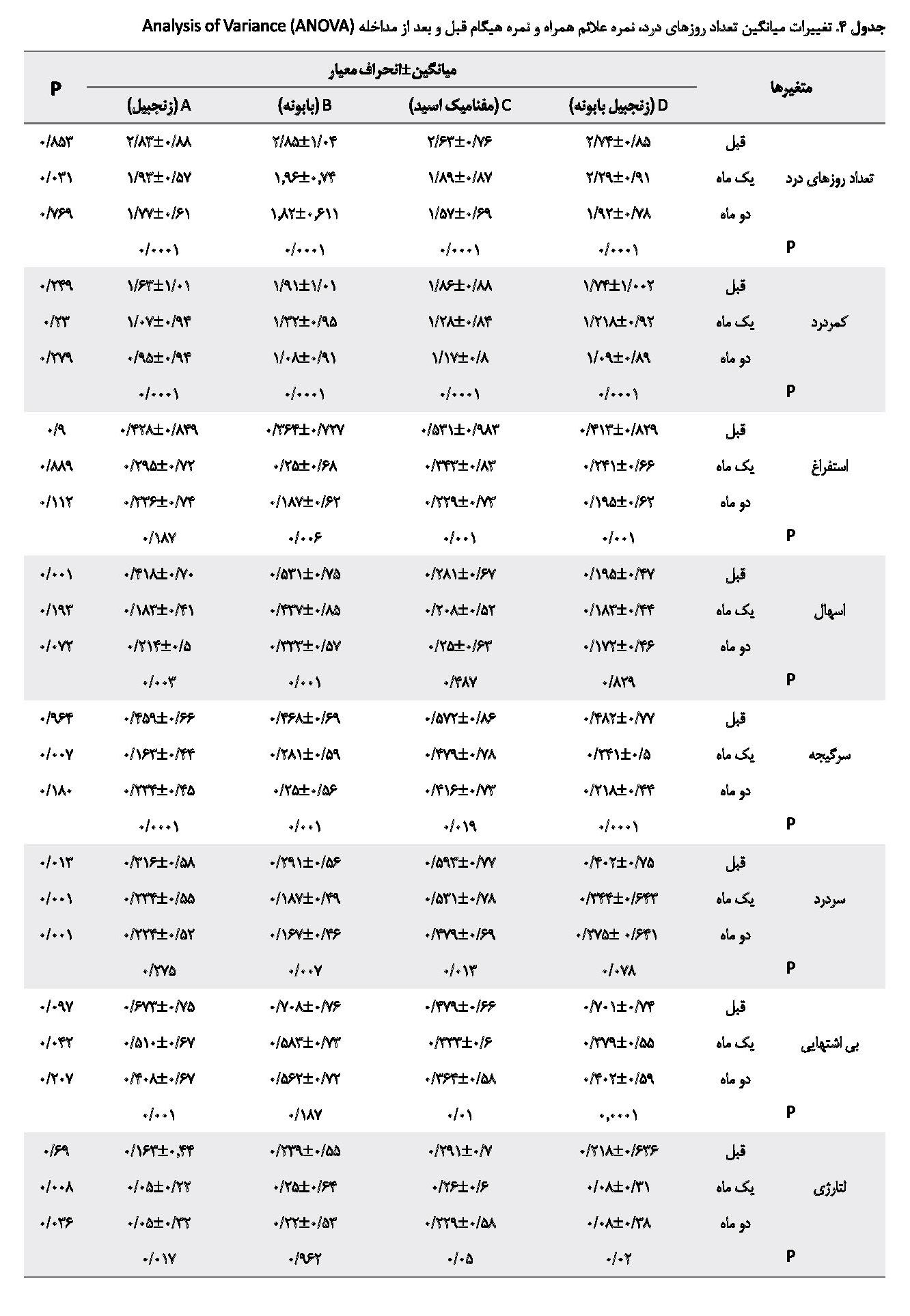
تفاوت کاهش سردرد و خستگی نیز یک و دو ماه بعد از مداخله بین گروهها معنادار بود. بیشترین تأثیر در کاهش خستگی مربوط به گروه زنجبیل و کمترین مربوط به گروه مفنامیک اسید بود (0/02=P). نتایج آزمون آنالیز واریانس نشان داد که میانگین نمره هیگام قبل از مطالعه در گروهها با یکدیگر اختلاف معنادار آماری داشته است. نتایج آنالیز کوواریانس نشان داد که میانگین نمره هیگام کاهشی بوده و دو ماه بعد بین گروهها با یکدیگر اختلاف معنادار آماری داشته است که بیشترین تغییر مربوط به گروه مفنامیک اسید و کمترین مربوط به زنجبیلـ بابونه بوده است (جدول شماره ۴).
بحث
نتایج مطالعه حاضر نشان داد که هر سه مداخله در کنترل درد در مقایسه با مفنامیک اسید، که جزء داروهای خط اول درمان دیسمنوره است، تأثیر مشابهی دارند. اما اگر مجموع درد تجربهشده بیماران را در نظر بگیریم، یعنی کمردرد و سردرد را هم در نظر بگیریم، تفاوتهایی رخ مینماید. در کنترل شدت درد، کاهش مصرف مسکن و نیز کاهش کمردرد هر چهار مداخله تأثیر مشابهی داشتند ولی در کنترل سردرد گروه زنجبیل و زنجبیل و بابونه تأثیر معناداری نداشتند و بابونه بهتر از مفنامیک اسید عمل کرده بود. بابونه به دلیل خاصیت مهار انتخابی آنزیم سیکلواکسیژناز 2 میتواند در تسکین درد و التهاب نقش مؤثری ایفا کند.
بابونه به دلیل خاصیت مهار انتخابی آنزیم سیکلواکسیژناز 2 می تواند در تسکین درد و التهاب نقش موثری ایفا کند [32]. دور از انتظار نیست که بابونه بتواند همسطح داروهای NSAIDs عمل کند، چراکه تأثیر آن در مهار انتخابی آنزیم COX-2 به اثبات رسیده است و با مکانیسمی مشابه NSAIDs در این زمینه عمل میکند. البته یافتههای این مطالعه درباره تأثیرنداشتن معنادار زنجبیل بر سردرد، با مطالعه کادی و همکاران در تضاد بود، چرا که در مطالعه ایشان بیان شده که زنجبیل به صورت معناداری در کنترل سردرد موفق بوده است [33]. بنابراین به نظر نمیرسد ترکیب بابونه و زنجبیل در کنترل تجربه درد بیمار مبتلا به دیسمنوره نسبت به بابونه برتری داشته باشد.
گرچه بابونه در کنترل درد نسبت به سایر مداخلات بهتر عمل کرده بود، در کنترل علائم و خـــــونریزی بهخوبی سایر مداخلات عمل نکرده بود و روی بعضی از علائم مثل بیحالی و بیاشتهایی نیز تأثیر معناداری نداشت. در حالی که جنابی و ابراهیمزاده در مطالعهای با بررسی تأثیر چای بابونه بر بهبود دیسمنوره اولیه به این نتیجه رسیدهاند که نوشیدن چای بابونه جهت تسکین درد قاعدگی ناشی از دیسمنوره اولیه و مشکلات روانی و اجتماعی آن مؤثر بوده است. در این مطالعه گروه مداخله، تا 3 ماه یک هفته قبل از قاعدگی تا روز 5 قاعدگی، هر روز 2 فنجان چای بابونه مصرف میکردند [15]. مطالعه شریفی و همکاران نیز نشان داده بود که بابونه نسبت به مفنامیک اسید در کنترل دردهای روانتنی مرتبط با دیسمنوره بهتر عمل میکند [34].
یزدانی و همکاران نیز تأثیر بابونه و رازیانه را بر دیسمنوره مطالعه کردهاند که در مطالعه آنها تأثیر این دو ترکیب بر درد، خستگی و مشکلات خلقی به اثبات رسیده است [35]. اما در مطالعه حاضر گرچه بابونه در کنترل درد بهتر عمل کرده بود، همچنان که ذکر شد در کنترل علائم خلقی ترکیب زنجبیل و بابونه و در کنترل خستگی زنجبیل بهتر عمل کرده بود. با توجه به اینکه یکی از سازوکارهای دخیل در بروز علائم خلقی نزدیک به قاعدگی کاهش نسبی سروتونین است [36]، میتوان نقش زنجبیل را در کنترل این علائم توجیه کرد، چراکه زنجبیل نیز حاوی ترکیباتی است مثل آگونیست که دستهای از رسپتورهای سروتونین است [37]. البته مکانیسم دقیق اختلالات خلقی نزدیک به قاعدگی هنوز مشخص نشده است و مکانیسمهای متعددی را در این موضوع دخیل میدانند، از جمله: افزایش تولید پروستاگلاندین ها [36].
با توجه به مهار انتخابی آنزیم COX-2 توسط بابونه [32] و کاهش تولید پروستاگلاندین به دنبال این اتفاق، باید از بابونه نیز تأثیرات مثبتی بر علائم خلقی انتظار داشت. درحالیکه این مطالعه منطبق بر این فرضیه نیست. برای توجیه این انطباق نداشتن، دو احتمال مطرح است: یک اینکه مکانیسمهای دیگری در تغییر خلق قبل از قاعدگی دخیل هستند، همچنان که بیان شد؛ دو این که دوز مورد استفاده در بروز این آثار نقش دارد که این احتمال نیز با مطالعات دیگری که تأثیر مثبت بابونه بر علائم خلقی را نشان دادهاند تقویت میشود، مثل مطالعه جنابی و همکاران [15] یا مطالعه یزدانی و همکاران [35].
نکته قابلتوجه دیگر در این مطالعه این است که دو گروه مصرفکننده زنجبیل در کنترل استفراغ نسبت به مفنامیک اسید و بابونه ضعیفتر عمل کرده بودند. گرچه زنجبیل به عنوان یکی از داروهای ضدتهوع و استفراع به دفعات در مطالعات بالینی استفاده شده است، هنوز شواهد کافی برای تأیید اثر آن وجود ندارد و در مورد دوز مؤثر آن بر تهوع و استفراغ نیز نیاز به مطالعات تکمیلی است [39، 38]. در مورد تأثیرات بابونه بر کنترل استفراغ مطالعات مؤید متعددی وجود دارد، ولی شواهد هنوز به حد مطلوب نرسیدهاند [38]. یکی دیگر از نکاتی که نباید از آن غافل بود، نقش عسل در تسکین دیسمنوره است که فراهانی و همکاران نیز آن را مطالعه و تأثیر آن را مشابه مفنامیک اسید ارزیابی کردهاند [40].
تاکنون مطالعهای به بررسی اثر ترکیب زنجبیل و بابونه همراه با عسل بر دیسمنوره نپرداخته است. در حال حاضر مطالعات بر روی ترکیبات دارویی رو به افزایش است، چراکه تکداروها در درمان بیماریهای مزمن موفقیت لازم را به دست نیاوردهاند. معمولاً ترکیبکردن داروها به هدف افزایش اثربخشی و کاهش عوارض صورت میگیرد. ترکیب چند دارو ممکن است اثر افزوده داشته باشند، مثل افزایش اثر دو داروی ضدسرفه بعد از ترکیبشدن، یا اینکه ترکیب باعث سینرژیسم شود، مثل افزایش طول اثر ضدسرفه یک دارو با افزودن یک داروی کاهنده متابولیسم، یا اینکه باعث کاهش آثار آنها شود، مثل ترکیب دو دارو که یکی متابولیسم دیگری را تسریع کند [41]. در مورد عصارههای جوشانده با آب جوش، باید انتظار داشته باشیم که برخی از فعل و انفعالات شیمیایی در بین ترکیبات طبیعی موجود در گیاهان جزء فرمول در طول جوشاندن اتفاق بیفتد. جوشانده ممکن است میزان استخراج عناصر فعال را تغییر داده و یا مواد مصنوعی جدید تولید کند که ممکن است فعالیتهای جدید دارویی را به نمایش بگذارد. این نوع اقدامات دارویی، که از ترکیب چندین گیاه در فرمول حاصل میشود ، «اثرات شیمیایی ترکیب شدن» نامیده میشوند. این اثرات میتواند در جهت مثبت یا منفی اتفاق بیفتد [42].
تاکنون مطالعهای به بررسی اثر ترکیب زنجبیل و بابونه همراه با عسل بر دیسمنوره نپرداخته است. معمولاً ترکیبکردن داروها به هدف افزایش اثربخشی و کاهش عوارض صورت میگیرد، ولی با توجه به مجموع نتایج بهدستآمده به نظر میرسد ترکیبکردن زنجبیل و بابونه باعث همافزایی آثار یا کاهش عوارض دارویی نشده باشد و این ترکیب برای درمان دیسمنوره برتری چشمگیری نسبت به زنجبیل یا بابونه یا عسل ندارد. ترکیب زنجبیل و بابونه در کنترل درد و علائم دیسمنوره در مقایسه با مفنامیک اسید، در بسیاری از جهات مشابه است، ولی این تأثیر نسبت به مصرف زنجبیل یا بابونه بهتنهایی برتری چندانی ندارد و در اکثر جهات مفنامیک اسید یا بابونه تنها یا زنجبیل تنها اثرات بهتری نیز داشتند، مثلاً گرچه زنجبیل و بابونه در کنترل شدت درد اندکی بهتر از گروههای دیگر عمل کرده بود (بدون تفاوت آماری معنادار) ولی در کاهش مدت زمان درد و تعداد روزهای درد، مفنامیک اسید، بابونه تنها و زنجبیل تنها بهتر بودند.
موضوع دیگر اینکه یکی از دلایلی که معمولاً برای ترجیح داروهای گیاهی مطرح میشود، گریز از عوارض داروهای NSAIDs است، ولی در این مطالعه مفنامیک اسید نسبت به سایر گروهها عارضه کمتری نشان داد. البته عوارض بلندمدت مفنامیک اسید را این مطالعه پیشبینی نکرده، همچنان که اثرات ترکیبات گیاهی استفادهشده نیز در بلندمدت نامعلوم است.
همانطور که در روش کار، جزئیات مطالعه را توضیح دادیم، سعی شد آثار عوامل مخدوشکننده مثل استرسهای غیرقابلاندازهگیری و مصرف چای، قهوه، نمک و شکلات با تصادفیسازی و متعیرهای مداخلهگر با همانندسازی به حداقل برسد. حجم نمونه نیز بیشتر از میزان مورد نیاز در نظر گرفته شد تا خطای انتخاب را کاهش دهیم و کورسازی برای محققان و بیماران برای کاهش خطای تفسیر دادهها صورت گرفت.
نتیجهگیری
با توجه به مجموع نتایج به استناد این مطالعه نمیتوان ترکیب زنجبیل و بابونه و عسل را نسبت به مفنامیک اسید یا زنجبیل و بابونه بهتنهایی ترجیح داد و به نظر میرسد این ترکیب باعث همافزایی آثار مثبت بابونه و زنجبیل و عسل نمیشود و شاید در بعضی موارد آثار آنها را تقلیل دهد. با وجود تصور عمومی مبنی بر همافزایی آثار گیاهان دارویی در ترکیب، باید دانست که این اتفاق به دلایل مختلف عملی نمیشود و تأثیر ترکیبات گیاهی باید همیشه نسبت به تکتک اجزای مؤثره آن مقایسه و مطالعه شود تا عوارض دارویی بیهوده به بیماران تحمیل نگردد.
یکی از محدودیتهای این پژوهش خوداظهاری نمونهها درباره فرایندهای طیشده در طی پژوهش بود که همیشه درجاتی از خطای خارج از کنترل را به همراه دارد. محدودیت دیگر این مطالعه این است که گروه کنترل بدون درمان در این مطالعه نبود و شبیهسازی ترکیبات گیاهی با مفنامیک اسید به طور کامل امکانپذیر نبود و راهی که انتخاب شد، استفاده از جعبههای مشابه برای قرار دادن داروها بود که محققان و بیماران از محتویات آن اطلاعی نداشتند.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این طرح با کد اخلاق ARAKMU.REC.1395.164 از کمیته اخلاق دانشگاه علوم پزشکی اراک و کد N52016100825031 در مرکز ثبت کازآزمایی های بالینی ثبت شده است.
حامی مالی
این مقاله حاصل طرحی تحقیقاتی است که با شماره 2611 در دانشگاه علوم پزشکی اراک به تصویب رسیده است و کلیه هزینههای آن را معاونت پژوهشی دانشگاه علومپزشکی اراک تأمین کرده است.
مشارکت نویسندگان
مفهومسازی، روششناسی و اعتبارسنجی: فاطمه شعبانی؛ تحلیل: محمدعلی زارعیان و فاطمه شعبانی؛ تحقیق و بررسی، منابع، نگارش پیشنویس، ویراستاری، نهاییسازی و بصریسازی: محمدعلی زارعیان؛ نظارت و مدیریت پروژه: فاطمه شعبانی.
تعارض منافع
بنابر اظهار نویسندگان این مقاله تعارض منافع ندارد.
تشکر و قدردانی
محققان از معاونت پژوهشی دانشگاه علومپزشکی اراک، شورای پژوهشی کمیته اخلاق دانشگاه، مرکز طب مکمل و کلیه مسئولان وکارکنان دانشگاه اراک و نیز تمامی شرکتکنندگان در این پژوهش کمال تشکر را دارند.
References
Novak E, Berek JS, Hillard PA, Adashi EY. Novak’s gynecology. 16th ed. New York: Lippincott Williams & Wilkins; 2019.
Xu L, Xie T, Shen T, Zhang T. Effect of Chinese herbal medicine on primary dysmenorrhea: A protocol for a systematic review and meta-analysis. Medicine. 2019; 98(38):e17191. [DOI:10.1097/MD.0000000000017191] [PMID] [PMCID]
Ju H, Jones M, Mishra G. The prevalence and risk factors of dysmenorrhea. Epidemiologic Reviews. 2013; 36(1):104-13. [DOI:10.1093/epirev/mxt009] [PMID]
Kharaghani R, Damghanian M. The prevalence of dysmenorrhea in iran: A systematic review and meta-analysis. Iranian Red Crescent Medical Journal. 2016; 19(3):e40856. [DOI:10.5812/ircmj.40856]
Osayande AS, Mehulic S. Diagnosis and initial management of dysmenorrhea. American Family Physician. 2014; 89(5):341-6.
Pattanittum P, Kunyanone N, Brown J, Sangkomkamhang US, Barnes J, Seyfoddin V, et al. Dietary supplements for dysmenorrhoea. Cochrane Database of Systematic Reviews. 2016; (3):CD002124. [DOI:10.1002/14651858.CD002124.pub2]
Jo J, Lee SH. Heat therapy for primary dysmenorrhea: A systematic review and meta-analysis of its effects on pain relief and quality of life. Scientific Reports. 2018; 8:16252. [DOI:10.1038/s41598-018-34303-z] [PMID] [PMCID]
Zhang F, Sun M, Han Sh, Shen X, Luo Y, Zhong D, et al. Acupuncture for primary dysmenorrhea: An overview of systematic reviews. Evidence-Based Complementary and Alternative Medicine. 2018; 2018:8791538. [DOI:10.1155/2018/8791538] [PMID] [PMCID]
McGovern CE, Cheung C. Yoga and quality of life in women with primary dysmenorrhea: A systematic review. Journal of Midwifery & Women’s Health. 2018; 63(4):470-82. [DOI:10.1111/jmwh.12729] [PMID]
Lee M, Lee H, Khalil M, Lim H, Lim HJ. Aromatherapy for managing pain in primary dysmenorrhea: A systematic review of randomized placebo-controlled trials. Journal of Clinical Medicine. 2018; 7(11):434. [DOI:10.3390/jcm7110434] [PMID] [PMCID]
Matthewman G, Lee A, Kaur JG, Daley AJ. Physical activity for primary dysmenorrhea: a systematic review and meta-analysis of randomized controlled trials. American Journal of Obstetrics and Gynecology. 2018; 219(3):255.E1-E-20. [DOI:10.1016/j.ajog.2018.04.001] [PMID]
Van Andel T, de Boer HJ, Barnes J, Vandebroek I. Medicinal plants used for menstrual disorders in Latin America, the Caribbean, sub-Saharan Africa, South and Southeast Asia and their uterine properties: A review. Journal of Ethnopharmacology. 2014; 155(2):992-1000. [DOI:10.1016/j.jep.2014.06.049] [PMID]
Shoja M, Joibari L, Sanagoo A. Ethno pharmacology study of herbs used for treatment of dysmenorrhea in northern Iran [Internet]. 2010 [Updated 2010 Jan 05]. Available from: http://www.goums.ac.ir/files/site1/abstract__persion.doc [Persian]
Ghaffari F, Mokaberi Nejad R, Moein E. Investigation of chamomile in traditional Iranian medicine literature. Avicenna Journal of Phytomedicine. 2015; 5(Suppl 1):92-3.
Jenabi E, Ebrahimzadeh S. [Chamomile tea for relief of primary dysmenorrhea (Persian)]. The Iranian Journal of Obstetrics, Gynecology and Infertility. 2010; 13(1):39-42. [DOI:10.22038/IJOGI.2010.5872]
Modarres M, Mirmohhamad Ali M, Oshrieh Z, Mehran A. [Comparison of the effect of mefenamic acid and matricaria camomilla capsules on primary dysmenorrhea (Persian)]. Journal of Babol University of Medical Sciences. 2011; 13(3):50-8.
Rafraf M, Zemestani M, Asghari-Jafarabadi M. Effectiveness of chamomile tea on glycemic control and serum lipid profile in patients with type 2 diabetes. Journal of Endocrinological Investigation. 2015; 38(2):163-70. [DOI:10.1007/s40618-014-0170-x] [PMID]
Rahimi M, Sanagoo A, Fatah ZA, Bahnampour N, Jouybari L. [Effect of chamomile tea on the severity of dyspnea and anxiety in patients with chronic heart failure: A clinical trial study (Persian)]. Journal of Gorgan University of Medical Sciences. 2018; 20(1):9-15.
Khan M, Ullah N, Azhar M, Komal W, Muhammad W. A mini-review on the therapeutic potential of Zingiber officinale (ginger). Natural Products: An Indian Journal. 2019; 15(1):125.
Santos Braga S. Ginger: Panacea or consumer’s hype? Applied Sciences. 2019; 9(8):1570. [DOI:10.3390/app9081570]
Azmoodeh E, Fazel N. [Dysmenorrhea and its treatment with chemical drugs and the highly used components of complementary and alternative medicine: A review (Persian)]. Beyhagh. 2009; 14(2):28-39.
Vahdatpoor H, Shakerian S, Alizadeh AA, Fatemi Tabatabaei SR. [The ginger supplementation effects on aerobic power training capacity and dysmenorrhea in overweight girls (Persian)]. Iranian Journal of Diabetes and Obesity. 2019; 11(2):93-8.
Pakniat H, Chegini V, Ranjkesh F, Hosseini MA. Comparison of the effect of vitamin E, vitamin D and ginger on the severity of primary dysmenorrhea: A single-blind clinical trial. Obstetrics & Gynecology Science. 2019; 62(6):462-8. [DOI:10.5468/ogs.2019.62.6.462] [PMID] [PMCID]
Omidvar S, Nasiri-Amiri F, Bakhtiari A, Begum Kh. Clinical trial for the management dysmenorrhea using selected spices. Complementary Therapies in Clinical Practice. 2019; 36:34-8. [DOI:10.1016/j.ctcp.2019.04.002] [PMID]
Rad HA, Basirat Z, Bakouei F, Moghadamnia AA, Khafri S, Kotenaei ZF, et al. Effect of ginger and novafen on menstrual pain: A cross-over trial. Taiwanese Journal of Obstetrics and Gynecology. 2018; 57(6):806-9. [DOI:10.1016/j.tjog.2018.10.006] [PMID]
Bogdanov S, Jurendic T, Sieber R, Gallmann P. Honey for nutrition and health: A review. Journal of the American College of Nutrition. 2008; 27(6):677-89. [DOI:10.1080/07315724.2008.10719745] [PMID]
Alvarez-Suarez JM, Tulipani S, Romandini S, Bertoli E, Battino M. Contribution of honey in nutrition and human health: A review. Mediterranean Journal of Nutrition and Metabolism. 2010; 3(1):15-23. [DOI:10.1007/s12349-009-0051-6]
Mirbagher Ajorpaz N, Hafezi M, Salehi S, Taybi A, Shenasa F, Zahtabehi S. [Comparing the effect of pure and impure honey on severity of pain, amount of bleeding, and duration and interval of menstrual cycles in female students with primary dysmenorrhea (Persian)]. Evidence Based Care Quarterly. 2012; 2(1):23-33. [DOI:10.22038/EBCJ.2012.379]
Wildemeersch D, Jandi S, Pett A, Hasskamp T. Management of primary dysmenorrhea in young women with frameless LNG-IUS. Journal of Contraception. 2014; 2014(5):23-8. [DOI:10.2147/OAJC.S52926]
Andresch B, Milsom I. An epidemiologic study of young women with dysmenorrheal. American Journal of Obstetrics and Gynecology. 1982; 144(6):655-60. [DOI:10.1016/0002-9378(82)90433-1]
Wyatt KM, Dimmock PW, Walker TJ, Shaughn O’Brien PM. Determination of total menstrual blood loss. Fertility and Sterility. 2001; 76(1):125-31. [DOI:10.1016/S0015-0282(01)01847-7]
Srivastava JK, Pandey M, Gupta S. Chamomile, a novel and selective COX-2 inhibitor with anti-inflammatory activity. Life Sci. 2009; 85(19-20):663-9. [DOI:10.1016/j.lfs.2009.09.007] [PMID] [PMCID]
Cady RK, Goldstein J, Nett R, Mitchell R, Beach ME, Browning R. A double‐blind placebo‐controlled pilot study of sublingual feverfew and ginger (LipiGesicTMM) in the treatment of migraine. Headache: The Journal of Head and Face Pain. 2011; 51(7):1078-86. [DOI:10.1111/j.1526-4610.2011.01910.x] [PMID]
Sharifi F, Simbar M, Mojab F, Alavi Majd H. Comparison of the effects of Matricaria chamomila (Chamomile) extract and mefenamic acid on the intensity of premenstrual syndrome. Complementary Therapies in Clinical Practice. 2014; 20(1):81-8. [DOI:10.1016/j.ctcp.2013.09.002] [PMID]
Yazdani M, Shahriari M, Hamedi B. Comparison of Fennel and Chamomile extract and placebo in treatment of premenstrual syndrome and dysmenorrheal. Hormozgan Medical Jouranl. 2004; 8(1):e90600.
Pearlstein T, Steiner M. Premenstrual dysphoric disorder: Burden of illness and treatment update. Focus. 2012; 10(1):90-101. [DOI:10.1176/appi.focus.10.1.90]
van Breemen RB, Tao Y, Li W. Cyclooxygenase-2 inhibitors in ginger (Zingiber officinale). Fitoterapia. 2011; 82(1):38-43. [DOI:10.1016/j.fitote.2010.09.004] [PMID] [PMCID]
Matthews A, Haas DM, O’Mathúna DP, Dowswell T. Interventions for nausea and vomiting in early pregnancy. Cochrane Database of Systematic Reviews. 2015; 9:CD007575. [DOI:10.1002/14651858.CD007575.pub4]
Nikkhah Bodagh M, Maleki I, Hekmatdoost A. Ginger in gastrointestinal disorders: A systematic review of clinical trials. Food Science & Nutrition. 2019; 7(1):96-108. [DOI:10.1002/fsn3.807] [PMID] [PMCID]
Farahani ËL, Hasanpoor-Azghdy SB, Kasraei H, Heidari T. Comparison of the effect of honey and mefenamic acid on the severity of pain in women with primary dysmenorrhea. Archives of Gynecology and Obstetrics. 2017; 296(2):277-83. [DOI:10.1007/s00404-017-4409-6] [PMID]
Che CT, Wang ZJ, Chow MSS, Lam CWK. Herb-herb combination for therapeutic enhancement and advancement: Theory, practice and future perspectives. Molecules. 2013; 18(5):5125-41. [DOI:10.3390/molecules18055125] [PMID] [PMCID]
Kiyohara H, Matsumoto T, Yamada H. Combination effects of herbs in a multi-herbal formula: Expression of Juzen-taiho-to’s immuno-modulatory activity on the intestinal immune system. Evidence-Based Complementary and Alternative Medicine. 2004; 1:363262. [DOI:10.1093/ecam/neh004] [PMID] [PMCID]
