مقدمه
آکانتامبا، آمیبی آزادزی است که بهفراوانی در محیط اطراف ما زندگی میکند. حضور این انگل در نمونههای آب، خاک، گرد و غبار و سیستمهای تهویه نقاط مختلف دنیا از جمله ایران تأیید شده است [1]. فراوانی این انگل امکان مواجهه انسان با آن را افزایش داده و از آنجا که این انگل فرصتطلب است، در صورت مناسببودن شرایط در بدن انسان ممکن است سلامت فرد را به خطر اندازد و به بیماری آکانتامبازیس (پوست، چشمی یا مغزی) منجر شود.
موارد مغزی این بیماری اغلب منجر به مرگ شده و درمان موارد چشمی نیز تا کنون چندان مؤثر نبوده است [2]؛ زیرا انگل در محیطهای برون و درونتنی به کیستهای بسیار مقاوم تبدیل میشود که مبارزه با آن را مشکل میکند [3]. در یک مطالعه 10ساله موارد بروز کراتیت آکانتامبایی در تهران 5/34 درصد گزارش شده است، ولی آماری از موارد عصبی در ایران وجود ندارد [4].
با اینکه طیف وسیعی از داروهای شیمیایی برای درمان این بیماری قابل استفاده است، ولی این داروها اثرات جانبی گوارشی، قلبیعروقی،کبدی و بینایی در انسان به جای میگذارند [6 ،5]. بنابراین جستوجو برای یافتن و جایگزینی داروهای طبیعی و سنتی به جای داروهای شیمیایی ادامه دارد [2]. امروزه اثر برخی از ترکیبات گیاهی در درمان این بیماری مطالعه و تأیید شده است. از جمله اثر عصاره آبی، الکلی و کلروفرمی گیاه گندواش در درمان آکانتامبازیس در محیط برون و درونتنی تأیید شده است [2]. همچنین اثر روغن درخت چای بر روی کیست و تروفوزوئیت آکانتامبا مطالعه و تأیید شده است [7]. از طرفی اثر کشندگی برخی از امواج مانند فراصوت و امواج الکترومغناطیسی مایکرو بر روی انگلهایی مانند پروتواسکولکسهای کیست هیداتیک، مطالعه شده است [9 ،8].
امواج الکترومغناطیسی غیریونیزه شامل امواج رادیویی و مایکرو هستند. امواج مایکرو از تلفنهای همراه، وایفای، بلوتوث اجاقهای پختوپز حاوی لامپ مگنترون و غیره حاصل میشوند. از آنجا که افراد از طریق منابع طبیعی و مصنوعی (ساخته شده توسط انسان) در معرض پرتو امواج با فرکانس بالای مایکرو قرار دارند، در سالهای اخیر بررسی اثرات آنها نهتنها بر روی انسان بلکه بر روی میکروارگانیسمها ( از جمله باکتریها) نیز مورد توجه قرار گرفته است [11 ،10]. به طوری که در برخی از مطالعات، از گرمای تولیدشده از امواج مایکرو برای درمان تومورهای بدخیم استفاده شده است [12].
با توجه به اینکه سنجش پتانسیل عوامل در دسترسی همچون طیفهای متفاوت امواج که در اطراف ما وجود دارد نهتنها میتواند به شناخت ما از عوامل محیطی بیفزاید، بلکه ممکن است منجر به یافتن روشهای جدید کنترلی یا درمانی ضد عوامل مولد بیماریها شود؛ بنابراین در این مطالعه به بررسی اثر امواج مایکرو بر روی کیستهای آکانتامبا در محیط برونتنی پرداخته شده است.
مواد و روشها
آمادهسازی کیستهای آکانتامبا
برای تهیه کیستهای آکانتامبا، یکی از سویههای بیماریزای انگل که در مطالعه میقانی و همکاران از خاک شهر اراک جدا شده و به ثبت بانک ژنی رسیده بود، درون پلیتهای حاوی محیط کشت آگار غیرمغذی همراه با باکتری اشرشیا کلی، کشت داده شد [13]. این پلیتها به انکوباتوری با دمای 28 درجه سلسیوس منتقل و از روز هفتم از نظر وجود کیست بررسی شدند [13]. پلیتهایی که انگل در آنها رشد کرده بود، توسط سرم فیزیولوژی شستوشو و کیستها از روی آنها جمعآوری شدند. کیستها به لوله آزمایش منتقل و سه بار با سرم فیزیولوژی شسته شدند. به منظور برآورد تعداد کیستهای آکانتامبا در هر میلیلیتر از سوسپانسیون انگلی از لام نئوبار استفاده شد. درنهایت سوسپانسیون انگلی حاوی 19 الی 20 هزار کیست انگل آکانتامبا در هر میلیلیتر، آماده شد. با توجه به قطر هر کیست آکانتامبا، رسوب کیستها حدود 10 الی 11 درصد از حجم هر میلیلیتر از سوسپانسیون انگلی را تشکیل میداد. این سوسپانسیون تا زمان آزمایش در دمای چهار درجه سانتیگراد در یخچال نگهداری شد.
بررسی مرگومیر انگل
به منظور بررسی مرگومیر کیستهای انگل آکانتامبا از رنگ ائوزین 0/1 درصد استفاده شد [14]. به این ترتیب که حجم مساوی از سوسپانسیون انگلی و رنگ ائوزین بر روی لام با هم مخلوط شده و پس از قراردادن لامل بر روی این لام، تعداد مرگومیر کیستها در 100 عدد انگل ثبت شد. کیستهای مرده رنگ را جذب میکردند، ولی کیست زنده بیرنگ باقی میماند (تصویر شماره 1).
آزمایشها
این مطالعه تجربی بر روی کیستهای انگل آکانتامبا در محیط برونتنی (لوله آزمایش) انجام شد.
به منظور تابش امواج مایکرو از یک دستگاه اون سامسونگ مدل ME3410W ساخت کشور کره جنوبی (Samsung Electronic Co.) استفاده شد. میزان قدرت امواج مایکرو در مرکز صفحه تابش ـ که نمونهها در این نقطه قرار داده میشدند ـ در حداکثر میزان یعنی 1550 وات و فرکانس امواج 2450 مگاهرتز بود. منبع قدرت دستگاه 220 ولت با فرکانس 50 هرتز و قدرت خروجی آن هزار وات بود [15]. به منظور سنجش دمای سوسپانسیون انگلی از ترمومتر دیجیتالی لوترون مدل 01(±0/1)-pT ساخت کشور تایوان استفاده شد [9].

مواجهه انگل با تابش پیوسته امواج مایکرو
8 عدد لوله اپندورف حاوی 100 میکرولیتر سوسپانسیون انگلی آماده شد. لولههای یک تا هشت به ترتیب به مدت صفر، 10، 30، 45، 60، 90، 105 و120 ثانیه تحت تابش پیوسته امواج مایکرو قرار گرفتند. پس از مواجهه، تعداد کیستهای مرده در 100 عدد انگل، شمارش و ثبت شد. لوله شماره 1 که مدت زمان تابش امواج به آن صفر بود، به عنوان گروه کنترل در نظر گرفته شد. هر آزمایش سهبار تکرار شد. دمای سوسپانسیون انگلی، قبل و بعد از تابش امواج ثبت شد و تفاوت دمای ابتدایی و انتهایی آزمایش به عنوان T∆ ثبت شد.
مواجهه انگل با تابش تکرارپذیر امواج مایکرو
هشت عدد لوله اپندورف حاوی 100 میکرولیتر سوسپانسیون انگلی آماده شد. لولههای یک تا هشت به ترتیب به مدت صفر،10 (s10×1)، 30 (s10×3)، 60 (s10×6)، 120(s20×6)، 180 (s30×6)، 270 (s45×6) و 360 (s60×6) ثانیه تحت تابش تکرارپذیر امواج مایکرو قرار گرفتند. دمای سوسپانسیون در ابتدای آزمایش اندازهگیری شد و پس از انجام تابش تا زمان بازگشت دما به حالت اولیه، تابش متوقف شده و سپس ادامه مییافت. پس از اتمام زمان مواجهه، تعداد انگلهای مرده، شمارش و ثبت شد. لوله شماره 1 که مدتزمان تابش امواج به آن صفر بود، به عنوان گروه کنترل در نظر گرفته شد. هر آزمایش سهبار تکرار شد.
تجزیه و تحلیل اطلاعات
تجزیه و تحلیل آماری با استفاده از نرم افزار SPSS و نسخه 16 اکسل انجام شد. به منظور بررسی نرمالیتی یافتهها از آزمون کولموگروف اسمیرنوف استفاده شد. میزان مرگومیر انگل به صورت میانگین مرگومیر در سهبار آزمایش مجزا ± انحراف معیار نشان داده شد. به منظور بررسی اختلاف بین گروهها با گروه کنترل از آزمون آماری One Way ANOVA استفاده شد. سطح معنیداری 05/0P< در نظر گرفته شد.
یافتهها
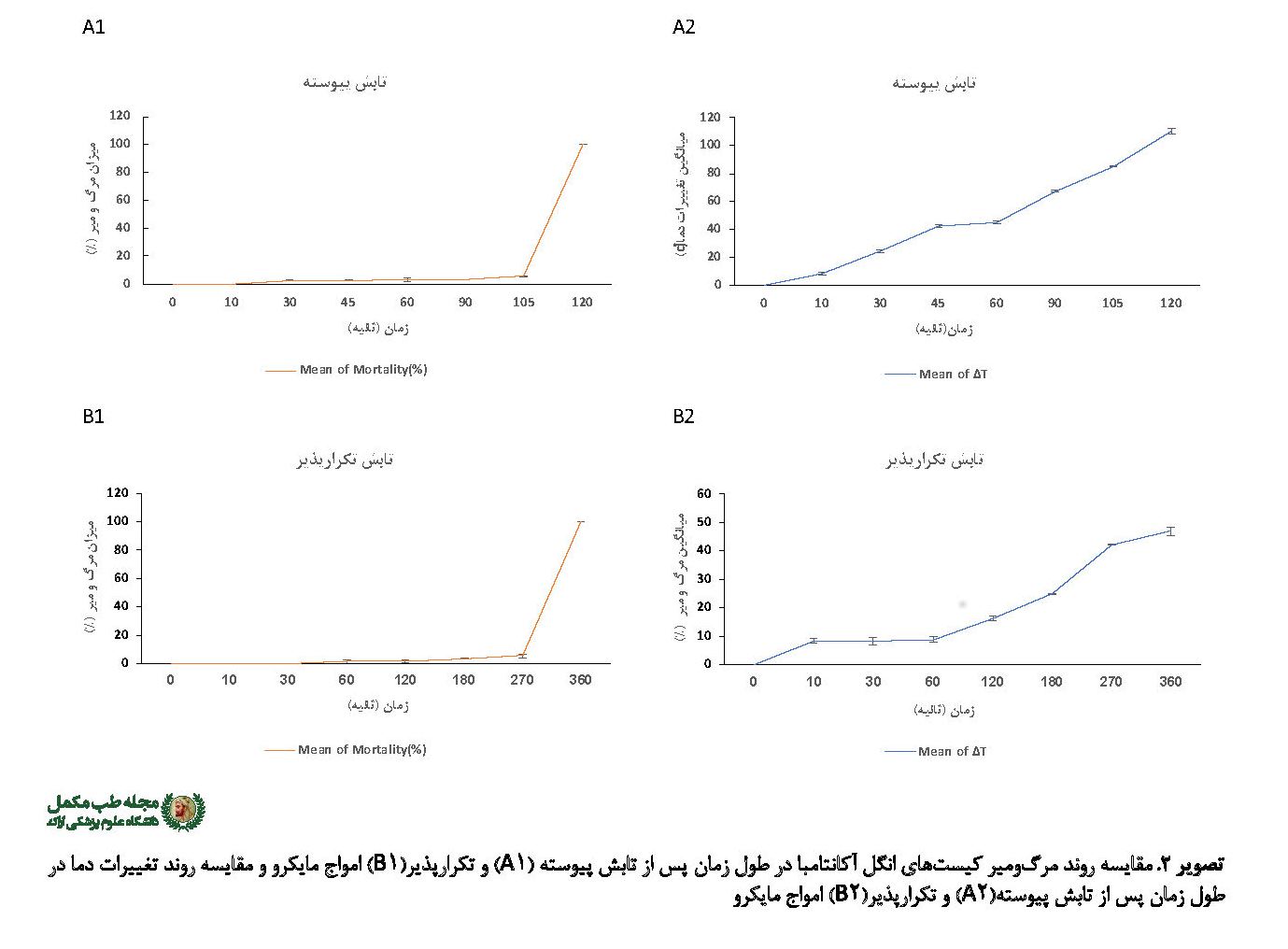
روند مرگومیر کیستهای آکانتامبا پس از تابش امواج مایکرو در تصویر شماره 2 مشاهده میشود. همچنین میزان مرگومیر کیستها پس از تابش پیوسته و تکرارپذیر امواج مایکرو به ترتیب در جداول شماره 1 و 2 نشان داده شده است. همانطور که در جدول شماره 1 مشاهده میشود پس از 105 ثانیه تابش امواج پیوسته، میزان مرگومیر کیستها 7/5 درصد بود، ولی پس از 120 ثانیه، مرگومیر به 100 درصد رسید.

همانطور که در جدول شماره 2 مشاهده میشود، پس از 270 ثانیه تابش امواج تکرارپذیر، میزان مرگومیر کیستها 5/3 درصد بود ولی پس از 360 ثانیه، مرگومیر به 100 درصد رسید. بر اساس نتایج آزمون کولموگروف اسمیرنوف یافتهها نرمال بودند.

آنالیز آماری تحلیل واریانس یکطرفه بین میزان مرگومیر کیستهای انگل آکانتامبا پس از تابش پیوسته امواج مایکرو که در جدول شماره 1 نشان داده شده است بیانگر این بود که در بین زمان تابش صفر ثانیه (گروه کنترل) با سایر زمانهای تابش (به جز 10 ثانیه) تفاوت آماری معنیدار وجود دارد (P<0/0001). همچنین آنالیز آماری نشان داد که میزان مرگومیر انگل در بین همه زمانهای تابش پیوسته به جز زمانهای 30 تا 90 ثانیه نسبت به یکدیگر نیز تفاوت معنیدار دارند (P<0/0001).
آنالیز آماری تحلیل واریانس یکطرفه بین میزان مرگومیر کیستهای انگل آکانتامبا پس از تابش تکرارپذیر امواج مایکرو که در جدول شماره 2 نشان داده شده است بیانگر این بود که در بین زمان تابش صفر (گروه کنترل) با همه زمانها به جز 10، 30 و 60 ثانیه تفاوت معنیدار وجود دارد (P<0/0001).
بحث
نتایج مطالعه کنونی که به منظور بررسی اثر کشندگی امواج مایکرو بر روی کیستهای انگل آکانتامبا انجام شد نشان داد که اثرات کشندگی این امواج وابسته به مدتزمان تابش امواج است.
آکانتامبا، ارگانیسمی پاتوژن است که مولد عفونتهای شدیدی مانند کراتیت و انسفالیت گرانولوماتوزی آمیبی است. حضور این انگل در محیط اطراف ما غیر قابل انکار است. این ارگانیسم جهانی در نمونههای خاک، هوا و آب و نیز بافتهای حیوانی شناسایی شده است [16]. این ارگانیسم قادر است به کیستهای مقاوم و خفته تبدیل شود که باعث شکست در درمان بیماریهای ناشی از این انگل میشود. به عبارت دیگر وجود کیستهای آکانتامبا علت مهم عدم کارایی داروهای رایج بر ضد این انگل است. کیستها در برابر داروهای شیمیایی مقاوماند و معمولاً برای اینکه این داروها مؤثر واقع شوند به دُز بیش از حد مجاز و طولانیمدت از داروها نیاز است که منجر به اثرات سمی روی سلول میشود؛ بنابراین یافتن و استفاده از داروهایی با منشأ طبیعی یا سایر روشهای درمانی که دیواره کیستی را از بین برده و یا مانع سنتز دیواره شود، مورد توجه قرار گرفته است [17].
تاکنون امکان استفاده از عصارهها و اجزای برخی گیاهان در درمان آکانتامبازیس بررسی شده یا در حال بررسی است [18].
مصرف برخی از این گیاهان در طب سنتی رایج است؛ زیرا خواص آنتیسپثیک یا ضدباکتریایی دارند. نتایج مطالعات نشان داده که ترکیبات برخی از این گیاهان از رشد آمیب ممانعت به عمل میآورند و برخی مانع کیستشدن آن میشوند. همچنین برخی از آنها فقط روی تروفوزوئیت اثر دارند و هیچ تأثیری بر روی کیستها ندارند [18]. خاصیت مطلوب عصارههای گیاهی، خاصیت آمیبواستاتیک و آمیبوسیدال (کشندگی آمیبی) آنها بر علیه تروفوزوئیتها و کیستهاست. تا سال 2016 گیاهی که روی هر دو شکل انگل مؤثر باشد، شناسایی نشده بود تا اینکه خاصیت تخریبکننده گیاه گندواش بر روی تروفوزوئیت و کیستهای این انگل به اثبات رسید [2].
نتایج مطالعاتی که بر روی اثر درمانی گیاهان و اجزای طبیعی آنها انجام شد، دانشمندان را تشویق کرد که به دنبال روشهای جدید یا ازقلمافتاده با خواص درمانی مناسب باشند. استفاده از خواص درمانی عوامل مکانیکی از جمله امواج نیز در سالهای اخیر مورد توجه قرار گرفته است.
دنیای امروز در معرض دائم امواج رادیویی و الکترومغناطیس حاصل از گوشی موبایل، مایکروفر و سایر دستگاههاست. اکثر محققان از عوارض خطرناک این امواج نگران هستند، ولی برخی از محققان به استفاده از این امواج جهت از بین بردن ارگانیسمهای بیماریزا و درمان بیماریها توجه نشان داده و پیشرفتهایی در این زمینه به دست آوردهاند. از جمله رایف و همکارانش نشان دادند که سلولهای نامطلوب (سرطانی) و میکروبها را میتوان با امواج رادیویی از بین برد، در حالی که این امواج بر روی سلولهای سالم بیتأثیر بودند [19]. به عبارت دیگر یکی از اولین کاربردهای پزشکی امواج الکترومغناطیسی جهت تخریب سلولهای سرطانی بوده است [20].
بررسی اثر امواج بر روی انگلها اخیراً آغاز شده است؛ به طوری که در برخی از مطالعات اثر امواج فراصوت با شدت بالا و امواج مایکرو بر روی پروتواسکولکسهای کیست هیداتیک بررسی و تأثیر آنها در افزایش مرگومیر انگل مذکور به اثبات رسیده است [15 ،9 ،8]. همچنین اثر امواج رادیویی در درمان بیماری انگلی کیست هیداتیک استفاده شده است؛ زیرا گرمای حاصل از این امواج باعث تخریب لایه زایای کیست و غیرفعال شدن آن میشود [22 ،21]. در مطالعه کنونی تأثیر این نوع موج به عنوان پرتو غیریونیزان با فرکانس بالا با اثرات گرمایی بر روی کیستهای بسیار مقاوم انگل آکانتامبا بررسی شد. در این مطالعه به اثبات رسید که اثر امواج مایکرو بر روی کیستهای آکانتامبا به مدت زمان تابش امواج بستگی دارد. از طرفی میزان مرگومیر انگل آکانتامبا در تابش پیوسته و تکرارپذیر امواج مایکرو به ترتیب در طی مدت 105 و 270 ثانیه از شش در صد تجاوز نکرد، ولی وقتی مدت تابش به ترتیب به 120 و 360 ثانیه افزایش یافت میزان مرگومیر سریعاً به 100 درصد رسید و تمام انگلها از بین رفت.
نتایج مطالعه کنونی نشان داد که در طی تابش پیوسته امواج مایکرو به مدت 105 ثانیه با اینکه اختلاف دمای ابتدایی تا انتهایی آزمایش به بیش از 83 درجه سانتیگراد رسید، میزان مرگومیر کیستهای آکانتامبا فقط 7/5 درصد بود. در حالی که در طی تابش امواج تکرارپذیر مایکرو به مدت 270 ثانیه که اختلاف دمای ابتدا و انتهای تابش حدود 42 درجه سانتیگراد بود، میزان مرگومیر انگل تقریباَ مشابه حالت پیوسته 3/5 درصد بود. به نظر میرسد که در این آزمایش گرمای حاصل از امواج بهتنهایی در افزایش مرگومیر انگل مؤثر نیست، بلکه خواص دیگر این امواج در مرگ کیستهای آکانتامبا نقش ایفا میکنند که برای شناخت این خواص نیاز به مطالعات بیشتری است.
نتیجهگیری
نتایج این مطالعه نشان داد که با اینکه تغییر در شیوه تابش امواج از نوع پیوسته به تکرارپذیر، تا حدودی اثرات دمایی امواج مایکرو را کاهش داده، ولی میزان مر گومیر کیست، تقریباً مشابه حالت پیوسته است. بنابراین به نظر میرسد تأثیر امواج مایکرو فقط ناشی از افزایش حرارت محیط نیست، بلکه خاصیت دیگری از این نوع موج نیز در مرگ انگل آکانتامبا دخالت دارد. البته مدتزمان لازم برای مرگ کیستهای آکانتامبا در حالت تکرارپذیر حدود سه برابر زمان حالت پیوسته بود. به منظور دستیابی به نتایج دقیقتر نیاز به تکرار این آزمایشات توسط امواجی با قدرت و فرکانس متفاوت در محیط برونتنی است. این تحقیق جهت بررسی اثر امواج مایکرو به عنوان پرتو غیریونیزان و با فرکانس بالا در محیط برونتنی انجام شده است و جهت ادامه آزمایشات در محیط درونتنی نیاز به انتخاب فرکانس بهینه در محدوده مایکرو و با توجه به شرایط محیط فیزیولوژیکی انتخابشده خواهد بود.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
این طرح پژوهش با کد اخلاق IR.ARAKMU.REC.1394.192 در کمیته اخلاق دانشگاه علومپزشکی اراک به تصویب رسیده است.
حامی مالی
این پژوهش با حمایت مالی معاونت تحقیقات و فناوری دانشگاه علومپزشکی اراک انجام شد.
مشارکت نویسندگان
نویسندگان به یک اندازه در نگارش پژوهش مشارکت داشتند.
تعارض منافع
نویسندگان مقاله تصریح میکنند هیچگونه تضاد منافعی در پژوهش حاضر وجود ندارد.
References
Niyyati M, Rezaeian M. Current status of Acanthamoeba in Iran: A narrative review article. Iranian Journal of Parasitology. 2015; 10(2):157-63. [PMID] [PMCID]
Derda M, Hadaś E, Cholewiński M, Skrzypczak Ł, Grzondziel A, Wojtkowiak-Giera A. Artemisia annua L. as a plant with potential use in the treatment of acanthamoebiasis. Parasitology Research. 2016; 115:1635-9. [DOI:10.1007/s00436-016-4902-z] [PMID] [PMCID]
Anwar A, Siddiqui R, Hameed A, Shah MR, Khan NA. Synthetic dihydropyridines as novel antiacanthamoebic agents. Medicinal Chemistry. 2019; 15:1. [DOI:10.2174/1573406415666190722113412] [PMID]
Feiz Haddad MH, Shokri A, Habibpour H, Heidar Nejadi SM. A review of Acanthamoeba keratitis in the Middle East and Iran. Journal of Acute Disease. 2019; 8(4):133-41. [DOI:10.4103/2221-6189.263705]
Müller GG, Kara-José N, de Castro RS. Antifungals in eye infections: Drugs and routes of administration. Revista Brasileira de Oftalmologia. 2013; 72(2):132-41. [DOI:10.1590/S0034-72802013000200014]
Siddiqui R, Aqeel Y, Khan NA. The development of drugs against acanthamoeba infections. Antimicrobial Agents and Chemotherapy. 2016; 60(11):6441-50. [DOI:10.1128/AAC.00686-16] [PMID] [PMCID]
Hadaś E, Derda M, Cholewiński M. Evaluation of the effectiveness of tea tree oil in treatment of Acanthamoeba infection. Parasitology Research. 2017; 116(3):997-1001. [DOI:10.1007/s00436-017-5377-2] [PMID] [PMCID]
Liu AB, Cai H, Ye B, Chen LL, Wang MY, Zhang J, et al. The damages of high intensity focused ultrasound to transplanted hydatid cysts in abdominal cavities of rabbits with aids of ultrasound contrast agent and superabsorbent polymer. Parasitology Research. 2013; 112(5):1865-75. [DOI:10.1007/s00436-013-3340-4] [PMID]
Eslamirad Z, Soleimani H, Hajihossein R, Rafiei F. Evaluation of lethal effect of microwave exposure on protoscolices of hydatid cyst in vitro. Asian Pacific Journal of Tropical Disease. 2015; 5(10):821-4. [DOI:10.1016/S2222-1808(15)60938-0]
Salmen SH, Alharbi SA, Faden AA, Wainwright M. Evaluation of effect of high frequency electromagnetic field on growth and antibiotic sensitivity of bacteria. Saudi Journal of Biological Sciences. 2018; 25(1):105-10. [DOI:10.1016/j.sjbs.2017.07.006] [PMID] [PMCID]
Ozdemir F, Kargi A. Electromagnetic waves and human health. In: Zhurbenko V, editor. Electromagnetic Waves. Rijeka: InTech; 2011. [DOI:10.5772/16343]
Cairang Y, Zhang L, Ren B, Ren L, Hou L, Wang H, et al. Efficacy and safety of ultrasound-guided percutaneous microwave ablation for the treatment of hepatic alveolar echinococcosis: A preliminary study. Medicine. 2017; 96(27):e7137. [DOI:10.1097/MD.0000000000007137] [PMID] [PMCID]
Meighani M, Eslamirad Z, Hajihossein R, Ahmadi A, Saki S. Isolation and genotyping of acanthamoeba from soil samples in Markazi Province, Iran. Open Access Macedonian Journal of Medical Sciences. 2018; 6(12):2290-4. [DOI:10.3889/oamjms.2018.454] [PMID] [PMCID]
El-Sayed NM, Hikal WM. Several staining techniques to enhance the visibility of Acanthamoeba cysts. Parasitology Research. 2015; 114:823-30. [DOI:10.1007/s00436-014-4190-4] [PMID]
Eslamirad Z, Soleimani H. [Investigating the potential of protoscolices for cyst formation under in vivo microwave radiation (Persian)]. Complementary Medicine Journal. 2019; 9(1):3598-606. http://cmja.arakmu.ac.ir/article-1-647-en.html
Mosayebi M, Hajihossein R, Ghorbanzadeh B, Kalantari S. A risk for nosocomial infection: contamination of hospital air cooling systems by Acanthamoeba spp. International Journal of Hospital Research. 2016; 5(1):17-21. [DOI:10.15171/ijhr.2016.04]
Anwar A, Khan NA, Siddiqui R. Combating Acanthamoeba spp. cysts: What are the options? Parasites & Vectors. 2018; 11:26. [DOI:10.1186/s13071-017-2572-z] [PMID] [PMCID]
Parasitology T, Ghaffarifar F, Fakhar M, Saberi R. Medicinal plants with anti-Acanthamoeba activity: A systematic review. Infectious Disorders - Drug Targets. 2019; 19:1. [DOI:10.2174/1871526519666190716095849] [PMID]
Atari Lar S, Ebrahimi M. [A reflection on the healing power of the waves (Persian)]. Journal of Vibration & Sound. 2018; 7(13):104-19. http://jvs.isav.ir/article_32705.html
Hedrick WR, Hykes DL, Strachman DE. Ultrasound physics and instrumentation. St. Louis: Mosby; 2005. https://books.google.com/books?id=QoVsQgAACAAJ&dq
Botsa E, Thanou I, Nikas I, Thanos L. Treatment of hepatic hydatid cyst in a 7-year-old boy using a new type of radiofrequency ablation electrode. The American Journal of Case Reports. 2017; 18:953-8. [DOI:10.12659/AJCR.904432] [PMID] [PMCID]
Du XL, Ma QJ, Wu T, Lu JG, Bao GQ, Chu YK. Treatment of hepatic cysts by B-ultrasound-guided radiofrequency ablation. Hepatobiliary & Pancreatic Diseases International. 2007; 6(3):330-2. [PMID]


 ، رضا حاجی حسین1
، رضا حاجی حسین1 

 ، هما سلیمانی
، هما سلیمانی 

 2
2
