مقدمه
یکی از فرضیات اصلی که با تسریع در روند سالمندی همراه است، نقص در عملکرد میتوکندری است. طی این فرضیه با از بین رفتن میتوکندری، مقادیر و عملکرد آنزیمهای زنجیره تنفسی میتوکندری کاهش و به دنبال آن مقادیر فشار اکسایشی در سلول افزایش مییابد.
این فرایند سبب تخریب سلولی و کاهش طول عمر به دنبال کاهش بیوژنز میتوکندری میشود [
1]. با وجود این، افزایش تنظیمکنندههای مهم (PGC-1α) میتوکندری از مسیرهای مختلف نقش مهمی در مهار ROS و بیوژنز میتوکندری دارد [
2].
بیوژنز میتوکندری فرایندی است که طی آن میتوکندری جدید در سلول تشکیل میشود. پیدایش حیات میتوکندری توسط تعداد زیادی سیگنالهای مختلف در زمان تحریک سلولی یا در پاسخ به محرکهای محیطی فعال میشود؛ بنابراین میتوکندری یک تنظیمکننده کلیدی از فعالیت متابولیک سلول و اندامکی مهم در تولید و تخریب رادیکالهای آزاد است که بیوژنز آن با محافظت از سلول و افزایش طول عمر همراه است.
PGC-1α یکی از مهمترین کواکتیویتورهای رونویسی است که به طور مثبتی بیان ژنهای مرتبط با سازگاریهای متابولیکی و میتوکندریایی را تنظیم میکند و درنتیجه بر عملکرد میتوکندری، ظرفیت تولید ATP و نیز تولید ROS تأثیر میگذارد [
3]. سالمندی میتواند بر پویایی (داینامیک) میتوکندری تأثیر داشته باشد [
4].
پویایی میتوکندریایی شامل فرایند شکاف و همجوشی است که مهمترین پروتئینهای همجوشی MFn1 هستند [
5]. کاهش پروتئینهای همجوشی در افراد سالمند موجب اختلال در عملکرد میتوکندری، ازدستدادن پتانسیل غشا، کاهش اکسیژن و افزایش تولید گونههای فعال اکسیژن میشود [
6].
عدم تعادل در پروتئینهای همجوشی MFn1 شکافت، باعث بههمریختگی ساختاری میتوکندری، اختلالات متابولیسمی تجزیه میتوکندریها، آپوپتوز و حتی مرگ سلولی میشود [
5].اختلال در عملکرد میتوکندری ممکن است نه تنها باعث تجمع چربی شود، بلکه ROS و سایتوکاینهای افزایش دهد [
4].
علاوه بر این، افزایش سن با افزایش رسوب کلاژن نیز همراه است [
8 ،
7]. رسوب کلاژن میتواند اولین تظاهر روندی باشد که سرانجام به سیرز منجر شود. برخی مطالعات نشان داده که کاهش MFn1 به افزایش رسوب کلاژن منجر میشود [
9].
مطالعات نشان داده که بهبود سبک زندگی، افزایش تحرک بدنی و همچنین استفاده از مکملهای غذایی میتواند سلامت میتوکندری را تضمین کند. انجام تمرینات ورزشی قادر به افزایش بیوژنز میتوکندری است و تمرینات مختلف به صورت متفاوتی بر میتوکندری تأثیرگذار باشند [
10].
انجام تمرینات ورزشی با افزایش مقادیر آنزیمهای آنتیاکسیدانی نظیر کاتالاز در بهبود عملکرد میتوکندریایی مؤثر است [
11]. با وجود این، در تحقیقات مختلف بیان شده است که تمرینات مختلف، تأثیرات متفاوتی بر جای میگذارند. در طی ورزش شدید، مصرف اکـسیژن در بدن حدود 13-1 برابر افزایش مییابد، به همـین دلیـل بـا افـزایش تولید رادیکال آزاد به علت افـزایش مـصرف اکـسیژن، ممکن است ظرفیت دفاع آنتیاکسیدانی بدن تـضعیف شود [
12].
بنابراین ورزش حاد و شدید منجر بـه افـزایش ROS میشود، اما سازگاری با آن (اثر مزمن ورزش) از طریـق افـزایش دفـاع آنتـیاکسیدانی منجر به کـاهش ROS خواهد شد [
12].
یکی از پاسخ هایی که بدن به کاهش ROS میدهد، افزایش بیوژنز میتوکندری است [
13]. همچنین برخی مطالعات نشان داده که ورزش تمرین مقاومتی باعث رسوب کلاژن در قلب میشود [
14]. تحقیقات دیگری به کاهش رسوب کلاژن کبدی در کبد چرب غیرالکلی در اثر هوازی اشاره کردهاند [
15].
از سوی دیگر، گزارش شده که مصرف ویتامین C، استرس اکسیداتیو را کاهش میدهد و در بسیاری از موارد، عملکرد فیزیولوژیکی را در انسان بالغ بهبود میبخشد. از دیگر فواید یادشده برای مصرف ویتامین C شامل افزایش حساسیت بارورفلکس [
16]، بهبود عملکرد قلبی عروقی [
18 ،
17]، کاهش التهاب سیستمیک و کاهش نیاز به مایعات در شرایط صدمات حرارتی [
19]، مقاومت در برابر خستگی در سنین بالا [
20] و همچنین خاصیت ضدسرطانی [
21] است. مطالعات دیگری نیز نشان داده که ویتامین C در افزایش تولید کلاژن در افزایش تولید کلاژن مؤثر است [
22].
در هر حال، کاهش بیوژنز میتوکندری یکی از عوامل اصلی در افزایش روند پیری و آسیبهای ناشی از آن بر بافتهای بدنی، بهویژه بافت کبدی است، که از طریق مختلفی مانند سازگاری با تمرینات ورزشی و مصرف آنتیاکسیدانها میتوان با آنان مقابله کرد.
مطالعات محدودی به بررسی نقش ویتامین C، بهویژه فرم لیپوزومال آن با تمرینات ورزشی پرداختهاند. از آنجا که تمرین ورزشی باعث بهبود بیوژنز میتوکندریایی و افزایش ظرفیت آنتیاکسیدانتی میشود و همچنین تأثیرات ویتامین C، بهویژه فرم لیپوزومال آن بر بهبود ظرفیت آنتیاکسیدانتی مورد تأیید قرار گرفته است؛ بنابراین هدف از پژوهش حاضر، بررسی تأثیر تمرین ورزشی و مصرف ویتامین C بر PGC-1α ،MFn1 و رسوب کلاژن موشهای صحرایی سالمند است.
مواد و روشها
پس از انتقال موشها به محیط آزمایشگاه و سازگاری با محیط جدید به مدت یک هفته، به صورت گروههای سه تایی در قفسهای پلیکربنات شفاف در محیطی با دمای 2±23 درجه سانتیگراد، رطوبت 45 تا 55 درصد و چرخه تاریکی به روشنایی 12:12 ساعته نگهداری شدند.
در طی پژوهش، غذای استاندارد پلت و آب به صورت آزاد در اختیار قرار گرفت. در این پژوهش، 25 موش صحرایی نر (نژاد ویستار) با گروه سنی 24 هفتهای (280-320 گرم) به صورت تصادفی (داشتن شانس برابر برای قرار گرفتن هر موش در هر گروه ) در پنج گروه پنج تایی در هر رده سنی به ترتیب زیر تقسیم شده و مورد مطالعه قرار گرفتند:
1) گروه «کنترل جوان» شامل پنج موش صحرایی جوان 6-8 هفتهای 220 تا 250 گرمی
2) گروه «سالمند+تمرین مقاومتی» شامل پنج موش صحرایی سالمند و تمرین بدنی
3) گروه «سالمند+ویتامین C لیپوزومال» شامل پنج موش صحرایی سالمند و ویتامین C لیپوزومال
4) گروه «سالمند+تمرین مقاومتی+ویتامین C لیپوزومال» شامل پنج موش صحرایی سالمند+تمرین مقاومتی+ویتامین C لیپوزومال
5) گروه «کنترل دوران سالمندی» شامل پنج موش صحرایی سالم سن 24 هفتهای
در گروه تمرین مقاومتی به مدت سه روز در هفته، هر روز بیست دقیقه تمرین مقاومتی با نردبان و وزنه، به مدت هشت هفته تمرین داده شد [
23]. پس از پایان مدت زمان تمرین جهت بررسیهای بعدی در هر گروه بررسی شد.
در گروههای دریافتکننده ویتامین C لیپوزومال، در هر گروه روزانه ویتامین C لیپوزومال (Dr. Mercola) به صورت گاواژ بر اساس کیلوگرم وزن بدن (صد میلیگرم / کیلوگرم / روز) تجویز شد [
24].
در هر گروه، وزن در ابتدا و انتهای مطالعه بررسی شد. موشها پس از بیهوشی، خونگیری و سپس کشته شدند سپس سرم خون جداسازی و درنهایت بافت مغزی برای انجام تستهای پاتولوژیکی و بررسی بیان آنزیم و ژن استفاده شد.
جهت بررسی میزان فیبروز بافت کبد، ابتدا نمونه بافت کبد در محلول ثابتکننده تثبیت شد. در این مرحله بعد از مرگ موجود زنده، فعالیت آنزیمهای درون سلولی باعث فاسد شدن و تخریب ساختمان سلولی و بافتی میشود؛ بنابراین برای جلوگیری از تغییرات پس از مرگ، نمونه بافتی جداشده از بدن بایستی بلافاصله داخل محلولهای ثابتکننده قرار گیرد. محلولهای ثابتکننده ضمن پیوند با پروتئینها، باعث غیرفعال شدن آنزیمها شده و از انهدام ساختمان سلولها و بافتها جلوگیری میکند.
سپس به ترتیب مراحل آبگیری با الکل، شفافسازی با گزیلل، آغشتگی با پارافین، قالبگیری و سپس برشگیری انجام میشود. به منظور آبگیری بافت، نمونه را به ترتیب در الکل 50 درصد، 70 درصد، 90 درصد و مطلق قرار داده شد. سپس نمونه، داخل محلولی به نام گزیلل قرار داده شد که آن نیز جایگزین الکل میشود.
در مرحله آغشتگی، نمونه را در داخل پارافین مذاب قرار داده تا داخل بافت نفوذ کند. نمونه آغشتهشده با پارافین در این مرحله، داخل قالب پر از پارافین مذاب قرار میگیرد. ضمن انجماد پارافین، نمونه نیز داخل آن باقیمانده و آماده مقطعگیری میشود. نمونه همراه با قالب پارافین توسط دستگاهی به نام میکروتوم به ضخامت پنج تا ده میکرون برش داده میشود.
همچنین به منظور بررسی سطح فیبروز بافتی از رنگآمیزی تری کروم ماسون استفاده میشود. درصد فیبروز بافتی در هر گروه به لحاظ آماری مقایسه میشود.
به منظور بررسی بیان ژنهای PGC-1α و MFn1 در بافت عضله، از روش qPCR استفاده شد. در این بررسی، از ژن رفرنس Gapdh به عنوان ژن کنترل استفاده شد و بیان سایر ژنها با آن مقایسه شد. به منظور انجام این تکنیک ابتدا طراحی پرایمر انجام شد و سپس RNA کل از بافتها استخراج شده و به cDNA تبدیل شد. سپس cDNA به روش PCR تکثیر شده و از نظر بیان ژنهای یادشده بررسی شد.
استخراج RNA به روش دستی با استفاده از ماده ترایزول تهیهشده از شرکت کیازیست و طبق پروتکل استاندارد موجود برای روش ترایزول انجام شد. سنتز cDNAها با استفاده از کیت سنتز cDNA پارس توس مشهد انجام شد.
شماره کاتالوگ یا Cat no.: A101161. همچنین طراحی پرایمرها با برنامه Generunner نسخه 6.5 انجام شد. علاوه بر این روش، PCR با استفاده از کیت BioFACT کره انجام شد: 2X Real-Time PCR Master Mix (including SYBR Green, High ROX). cat no. DQ385-40h (جدول شماره 1، تصاویر شماره 1 و 2).

.PNG)
.PNG)
پروتکل تمرین مقاومتی
تمرین قدرت مستلزم این بود که موشها از نردبان یک متری با شبکه دو سانتیمتر تمایل به 85، با برخی تغییرات طبق شفر و همکاران صعود کردند [
26 ،
25]. موشها به مدت یک هفته با تمرین داده شده آشنا شدند. سپس، تمرین مقاومت شروع شد. برای این پروتکل، سیلندرهای حاوی وزنه با نوار فوم به پایه دم موش وصل شده بودند.
سیلندرها با پیچیدن قسمت بالایی دم (2-3 سانتیمتر از انتهای خارجی) با Velcro در بالای نوار فوم به دم بسته شدند. سپس، وزنههای اولیه (25 درصد از وزن بدن) وارد سیلندرها شدند. موشها سپس در پایه دستگاه کوهنوردی قرار گرفته و به صورت دستی برای بالا رفتن از نردبان تحریک شدند. وزن متصل به دم به تدریج طی هشت هفته تمرین (هفتههای یک و دو ، 50 درصد، هفتههای سه و چهار، 50 درصد، هفتههای پنج و شش، 75 درصد، هفته هفت و هشت به 100 درصد از وزن کل افزایش یافته است).
تمرینات سه تا پنج ست بین 8-12 تکرار، با استراحت یک دقیقه بین تکرارها و استراحت دو دقیقهای بین سِتها، به مدت سه یا چهار روز در هفته انجام شد. هر جلسه 40-50 دقیقه، با فاصله 48 ساعت بین جلسات انجام شد. پس از رسیدن به بالای نردبان، به موشها اجازه داده شد تا در منطقه استراحت ریکاوری کنند. این روش تا زمانی که موشها سه مجموعه تمرین را تمام کردند یا آنها نتوانستند طول کل نردبان را صعود کنند، تکرار شد [
25].
روش هیستوشیمیایی برای بررسی کلاژن
در این روش از رنگ هماتوکسیلین که از مغز چوب درخت بقم (لاگ وود) به دست میآید و با روش مخصوص که در ذیل آمد به صورت محلول ساخته میشود و هسته را رنگ میکند و ائوزین که قسمتهای دیگر بافت کبد را رنگ میکند، استفاده میشود. هزار سانتیمتر مکعب آب مقطر را در ارلن ریخته، روی اجاق گذاشتیم تا به جوش آید، سپس از روی اجاق برداشته به آرامی پودر آلن دوپتاس را در آن ریخته و مجدداً روی اجاق گذاشته، به هم زدیم تا کاملاً حل شود.
پودر هماتوکسیلین را در پنجاه سانتیمتر مکعب الکل اتیلیک 96 درجه حل کرده و دمای محلول آلن دوپتاس و آب را به حدود 85 درجه میرسانیم، سپس محلول هماتوکسیلین را روی آن میریزیم و به هم زده و بعد از اضافه کردن پودر اکسید مرکوریک ظرف را زیر شیر آب سرد قرار داده و ضمن به هم زدن به وسیله میله شیشهای سریع سرد میکنیم، سپس ده سانتیمتر مکعب اسید استیک گلایسیال اضافه کرده، 24 ساعت میگذاریم و بعد از آن قابل مصرف است. ضمناً نگهداری آن در شیشههای تیره مناسب است.
مواد و روشها
در این تحقیق، برای بررسی طبیعی بودن توزیع دادهها از آزمون شاپیرو ویلک استفاده شد. بعد از طبیعی بودن توزیع دادهها، از آزمون آنالیز واریانس یکطرفه برای بررسی تفاوت بینگروهی و از آزمون تعقیبی توکی برای مشخص کردن محل اختلاف گروهها استفاده شد. تمامی بررسیها با استفاده نرمافراز SPSS نسخه 22 و در سطح 0/05 ≥α انجام شد.
یافتهها
یافتههای این تحقیق از طریق آزمون آنوا نشان داد که در بین گروهها از نظر بیان PGC-1α تفاوت معناداری وجود دارد (0/001=P). نتایج آزمون تعقیبی نیز نشان داد که بین گروه موشهای صحرایی سالمند و گروه جوان تفاوت معناداری وجود دارد و مقدار PGC-1α در گروه جوان بیشتر است (0/001=P).
همچنین بین گروه سالمند با گروه سالمند تمرین همراه با مصرف ویتامین C نیز تفاوت معناداری مشاهده شد و این گروه در مقایسه با گروه سالمند از مقدار بیشتر PGC-1α برخوردار بود (0/001=P). بین سایر گروهها تفاوت معناداری مشاهده نشد.
همچنین نتایج آنوا نشان داد که بین گروهها از نظر MFn1 تفاوت معناداری وجود دارد (0/001=P). به نحوی که آزمون تعقیبی نشان داد که گروه موشهای صحرایی جوان از مقدار بیشتر MFn1 در مقایسه با گروه سالمند برخوردار بود (0/001=P).
بین گروه سالمند با گروه سالمند همراه با تمرین مقاومتی (0/71=P)، بین گروه سالمند با گروه سالمند همراه با ویتامین C لیپوزومال (0/82=P)، بین گروه سالمند با گروه سالمند همراه با تمرین مقاومتی و ویتامین C لیپوزومال (0/13=P) تفاوت معناداری از نظر MFn1 مشاهده نشد.
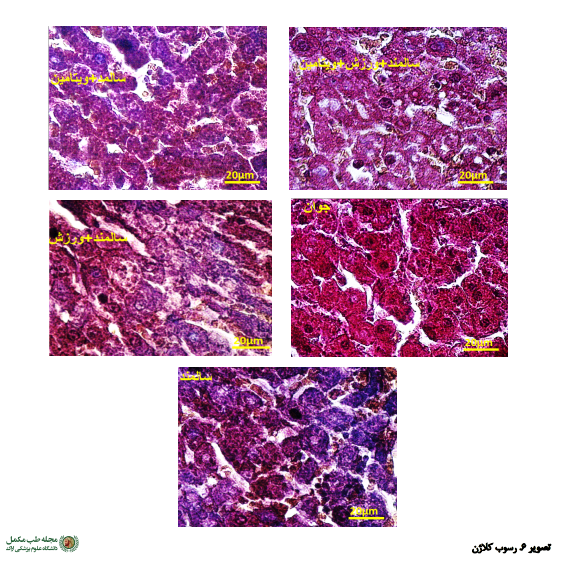
در مورد رسوب کلاژن نیز نتایج آزمون آنوا نشان داد که بین گروهها تفاوت معناداری وجود دارد (0/001=P). از طریق آزمون تعقیبی مشخص شد که بین گروههای سالمند همراه با تمرین، سالمند همراه با ویتامین، سالمند همراه با ویتامین و تمرین و جوان با گروه سالمند تفاوت معناداری وجود داشت (0/001=P) (
تصویر شماره 3).
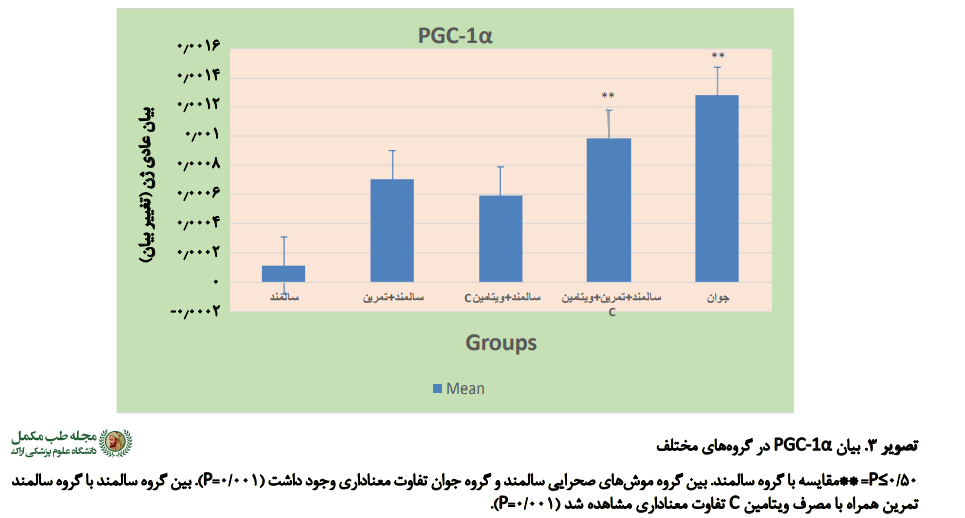
تفاوت بین گروه سالمند همراه با ویتامین و تمرین و گروه جوان با گروه سالمند همراه با تمرین معنادار بود (0/001=P). تفاوت بین سالمند همراه با ویتامین و تمرین و گروه جوان با گروه سالمند همراه با ویتامین نیز معنادار بود (0/001=P). تفاوت بین گروه سالمند همراه با ویتامین و تمرین با گروه جوان هم معنادار بود (0/001=P) (تصاویر شماره
4،
5 و
6).


 بحث
بحث
تحقیق حاضر با هدف اثر بررسی تأثیر تمرین ورزشی و مصرف ویتامین C بر PGC-1α و MFn1 موشهای صحرایی سالمند انجام شد. نتایج نشان داد که سالمندی باعث کاهش معنادار PGC-1α و MFn1 میشود. تمرین مقاومتی به همراه و مصرف ویتامین C باعث افزایش معنادار PGC-1α شد، اما MFn1 افزایش معناداری نیافت.
همچنین نتایج نشان داد که تمرین مقاومتی و مصرف ویتامین C به تنهایی تأثیر معناداری بر PGC-1α و MFn1 در بافت کبد موشهای صحرایی سالمند ندارد. همچنین نتایج این تحقیق نشان داد که انجام تمرین مقاومتی و مصرف ویتامین C به تنهایی میتواند بر کاهش رسوب کلاژن در موشهای صحرایی سالمند مؤثر باشد، اما اثر ترکیبی از تمرین مقاومتی و مصرف ویتامین C به نتایج بهتری منجر شد.
در همین راستا، دمیرچی و همکاران نشان دادند که تمرین تناوبی باعث افزایش معنادار PGC-1α و MFn1 در بافت قلب موشهای صحرایی نر مبتلا به انفارکتوس میوکارد میشود. دلروز و همکاران گزارش کردند که تمرین هوازی به همراه مصرف رزوراترول باعث افزایش MFn1 در میوسیتهای قلب در مدل حیوانی کبد چرب غیرالکلی میشود [
27].
دیگر مطالعات نیز نشان داد که ورزش تمرین مقاومتی باعث رسوب کلاژن در قلب میشود [
14]. کاهش رسوب کلاژن کبدی در کبد چرب غیرالکلی در اثر هوازی نیز گزارش شده است [
15].
تمرین مقاومتی و مصرف ویتامین از طریق مختلف، مانند کاهش فشار اکسایشی و کاهش عوامل التهابی همچون IL-6 و TNF-a میتواند بر کاهش رسوب کلاژن مؤثر باشد [
15 ،
14].
از سوی دیگر، نقش PGC-1α نیز حائز اهمیت است. ونز و همکاران (2009) گزارش کردند که افزایش PGC-1α به کاهش رسوب کلاژن عضلانی و کاهش فیبروزیس منجر میشود [
28].
از آنجا که تمرین مقاومتی به همراه مصرف ویتامین C باعث افزایش PGC-1α شد، این امکان وجود دارد که از این طریق، باعث کاهش رسوب کلسیم شده باشد. از سوی دیگر PGC-1α موجب بهبود عملکرد میتوکندری و بیوژنز میشود. تنظیم PGC-1α در سطح پروتئین و mRNA در پاسخ به تمرین از طریق تنوع گستردهای از سیگنالهای محیطی و آبشارهای سیگنالی درونسلولی مانند cAMP، AMPK و sirt1 انجام میگیرد [
29].
PGC-1α به عنوان هماهنگکننده فعالیت ژنهای درگیر در بیوژنز میتوکندریایی عضله اسکلتی هنگام تمرین معرفی شده [
30] و نشان داده شده است که PGC-1α سبب افزایش فعالیت ژنهای کدکننده آنزیمهای مسیر بتا اکسیداسیون اسید چرب از طریق فعالکننده کمکی فاکتور رونویسی PPARα میشود. فعالیت پروتئین کیناز فعالشده توسط (AMP (AMPK بیان PGC-1α را افزایش میدهد و افزایش فعالیت NRF-1 و بیوژنز میتوکندریایی را در پی دارد [
31].
مطالعات اندکی در زمینه آثار تمرینات ورزشی بر داینامیک میتوکندری وجود دارد و مکانیسم دقیق کنترل بازسازی میتوکندری به وضوح مشخص نیست. به نظر میرسد گونههای اکسیژن فعال نقش تنظیمکنندگی مهمی در این فرایند داشته باشند. ROS میتوکندریایی ناشی از فعالیت ورزشی میتواند به تغییر سریع در بیان پروتئینهای همجوشی و شکافت میتوکندریایی منجر شود [
32].
مطالعات انجامشده نشان داده که PGC-1α در سازگاری و پاسخ به فعالیت ورزشی به عنوان یکی از مهمترین تنظیمکنندهها نقش دارد. تنظیم داینامیک میتوکندری تحت تأثیر تنظیمکنندههای متابولیکی درون سلولی است که PGC-1α یکی از مهمترین تنظیمکنندههای متابولیسم انرژی و نیز بیوژنز میتوکندری است که در بازسازی میتوکندریایی از طریق تأثیر بر همجوشی و شکافت نقش دارد.
در همین راستا برخی مطالعات نشان داده که فعالیت ورزشی حاد منجر به افزایش بیان mRNA و سطوح پروتئینی MFn1 در عضله اسکلتی میشود که همراستا با افزایش PGC-1α است [
33].
مطالعات آزمایشگاهی نشان داده که بیان MFn1 به طور قابل توجهی در سلولهای عضلانی فاقد PGC-1α کاهش مییابد [
34]، در حالی که افزایش بیان PGC-1α منجر به تحریک بیان mRNA و پروتئین MFn1 در سلولهای عضلانی کشتشده میشود [
35].
هرچند در تحقیق حاضر افزایش PGC-1α در اثر ورزش و مصرف ویتامین C، تأثیر معناداری بر MFn1 نداشت، این احتمال وجود دارد که تغییرات MFn1 در بافتهای مختلف متفاوت باشد و یا عوامل دیگری به غیر از PGC-1α بر سطوح MFn1 مؤثر باشد که در این تحقیق بررسی نشده است. به عبارت دیگر، افزایش PGC-1α لزوماً به معنای افزایش MFn1 نیست.
چنانچه فینگ و همکاران [
36] و واکلزما و همکاران [
37]بیان کردند که فعالیت ورزشی طولانی مدت باعث کاهش مقدار MFn2 میشود. احتمالاً تفاوت در نوع آزمودنیها، شدت، مدت و نوع بافت تشریحشده از دلایل متفاوت نتایج باشد.
همچنین، بیش بیان PGC-1α و مسیرهای بیوژنز میتوکندری ناشی از فعالیت ورزشی حساس به ردوکس سلولی هستند، به طوری که مهار ROS بیان PGC-1α و بیان ژنهای بیوژنز میتوکندری کنترلشده با PGC-1α عضله اسکلتی را کاهش میدهد [
38].
نتیجهگیری
درنهایت میتوان نتیجه گرفت که تمرین مقاومتی به همراه مصرف ویتامین C در موشهای صحرایی سالمند باعث کاهش رسوب کلاژن در بافت کبد و نیز افزایش بیان PGC-1α میشود.
ملاحظات اخلاقی
پیروی از اصول اخلاق پژوهش
کمیته اخلاق پژوهشگاه تربیت بدنی و علوم ورزشی این مقاله را تأیید کرده است (کد اخلاق: IR.SSRI.REC.1399.775). اصول اخلاقی تماماً در این مقاله رعایت شده است. شرکت کنندگان اجازه داشتند هر زمان که مایل بودند از پژوهش خارج شوند. همچنین همه شرکت کنندگان در جریان روند پژوهش بودند. اطلاعات آن ها محرمانه نگه داشته شد.
حامی مالی
این مقاله مستخرج از رساله دکتری نویسنده اول در دانشکده تربیت بدنی دانشگاه آزاد اسلامی واحد تهران مرکز می باشد.
مشارکت نویسندگان
مفهومپردازی، روششناسی، نگارش-بررسی و ویرایش: همه نویسندگان. تحقیق ، نگارش-پیش نویس اصلی ، حمایت مالی: مصطفی خدابنده، و مقصود پیری؛ منابع: مقصود پیری وحسن متینهمایی.
تعارض منافع
نویسندگان این مقاله هیچگونه تعارض منافع ندارند.

.PNG)
.PNG)




